中国gcp和ICH-gcp的区别
目前国际通行的gcp是ICH-gcp,我国执行的是国家食品药品监督管理局(SFDA)颁布的中国gcp。中国现行gcp是2020年颁布,与ICH-gcp相比,具有中国特色。中国gcp是以ICH-gcp为蓝本,结合我国的实
来源:医疗器械注册代办 发布日期:2023-12-02 阅读量:次
随着医学和药物研发领域的不断发展,越来越多的专业人士开始关注和选择参与临床试验管理。其中,GCP(Good Clinical Practice)证书成为许多从业者追求的资格之一。然而,想要成功获得GCP证书并非轻而易举,因为在报考过程中有一系列的条件需要满足。以下是关于GCP证书报考条件的一些重要信息和建议。

一、学历要求
GCP证书报考并没有过于严格的学历要求,大多数考试机构仅要求报考者具备相关学历即可。尽管如此,建议报考者拥有医学、生物医学、药学等相关专业的学历背景,这将有助于更好地理解和掌握GCP的相关知识。毕竟,专业的学科背景能够为学习和应用GCP提供更为坚实的基础。
二、工作经验要求
通常情况下,GCP证书的报考机构要求报考者在医药临床试验管理、药物研发、医学数据分析等领域具有一定的工作经验。一般来说,最好是在相关领域工作一年以上。实际的工作经验不仅有助于深入理解GCP的相关知识和技能,还能够为报考者在职业生涯中更好地应用所学。

三、英语能力要求
GCP证书涉及许多英语专业名词,因此报考者需要具备一定的英语能力,包括英语听说读写能力和医学英语词汇量等方面的能力。在报名前,建议报考者提前准备,通过提高英语水平来确保能够流利地理解和运用GCP的知识。这对于顺利通过GCP的考试认证至关重要。
四、培训要求
在报考GCP证书前,通常需要接受相关的培训。报考者可以选择在线培训或现场培训,通过系统学习GCP的相关知识和技能。在选择培训机构时,要注意其资质和信誉度,以免因培训质量不佳而浪费时间和金钱。通过系统培训,报考者将更有信心和准备,成功通过GCP的考试认证。
总体而言,GCP证书的获得对于从事医学临床试验管理的专业人士至关重要。通过满足学历、工作经验、英语能力和培训等条件,报考者将更有可能取得成功。因此,在考虑报考GCP证书时,建议报考者充分了解相关要求,并在备考过程中做好充分准备,以确保能够在竞争激烈的领域中脱颖而出。

站点声明
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
思途医疗科技有限公司专注于医疗器械产品政策与法规规事务服务,提供产品注册备案申报代理、临床试验、体系建立辅导、分类界定、申请创新办理服务。

目前国际通行的gcp是ICH-gcp,我国执行的是国家食品药品监督管理局(SFDA)颁布的中国gcp。中国现行gcp是2020年颁布,与ICH-gcp相比,具有中国特色。中国gcp是以ICH-gcp为蓝本,结合我国的实

GMP、GLP和gcp是什么?GMP(GOOD MANUFACTURING PRACTICE)良好生产规范:世界卫生组织将GMP定义为指导食物、药品、医疗产品生产和质量管理的法规。GMP要求制药、食品等生产企业应具备良好的

gcp证书会过期吗?针对这个问题,特地查询了目前我国所有的临床现行法律法规,都没有发现gcp证书有效期的规定。对于gcp证书的更新问题,业内有传言五年一延续的说法,下面一起来

1.试验用医疗器械的研制应当符合适用的医疗器械______相关要求。A.质量管理体系B.风险管理C.经营管理体系D.使用管理体系

gcp证书有用吗?有用有用非常有用,gcp证书是临床行业的的准入门槛,也就是说,想要从事临床试验,必须要持有gcp证书。gcp证书适用人员gcp不但适用于即将或已经取

ICH-gcp是药品国际注册中共认的gcp。ICH-gcp列出的13条基本原则是gcp的科学性和伦理性原则的集中体现,是ICH-gcp的精华所在。随着我国药品审评审批制度改革的深入推进,我国gcp与ICH-gcp全面接

新版gcp的SAE/SUSAR怎么上报?先来了解一下什么是SAE?什么是SUSAR?跟随小编的脚步一起看看SAE和SUSAR的关系,最后再来探讨上报。正文如下:
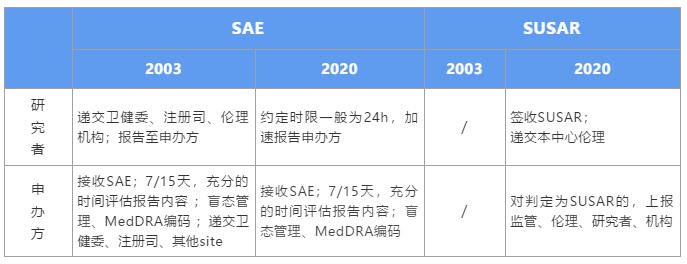
新版gcp对于申办方的影响是全方位的,就SAE个例报告处理方面,强化了申办方的主体责任,细化了申办方对SAE的管理流程。在此,我们详细解读,在新规之下,该如何高效、合规的处理

感谢作者的辛勤付出,文章全篇关于gcp的点点滴滴,文章字数有点多,需要您耐心观看,看完受益匪浅。

想考gcp证书,有什么培训机构靠谱,谢谢!?线上的比如:高研院gcp和思途,双方的流程都一样,不一样的在于,一个发的是高研院gcp证书,一个发的是药学会gcp证书,对想从事临床相
六年
医疗器械服务经验
联系思途,免费获得专属《落地解决方案》及报价
咨询相关问题或咨询报价,可以直接与我们联系
思途CRO——医疗器械注册临床第三方平台