网上销售情趣用品需要什么资质?什么证?
成人用品大多属于二类医疗器械,在网络销售成为情趣用品销售主要渠道的今天,除了办理二类医疗器械经营备案凭证之外,在网上销售情趣用品还要办理什么证吗?"
来源:医疗器械注册代办 发布日期:2026-01-05 阅读量:次
眼看注册证快到期了,延续申请提上日程。准备材料时,大家最常纠结的一个问题就是:当年为了拿证,花了一大笔钱做的那些产品检验报告,都好几年了,这次延续还能用吗?是不是所有检验都得重做一遍?重做的话,时间、样品、费用,都是不小的负担。不重做,又怕审评老师不认,卡住续证。这份钱到底该不该花,时间该怎么安排,心里实在没底。

别慌,这事儿有明确的规矩,也有灵活的空间。咱们先记住一个核心原则:延续注册,审的是你过去这五年里,产品的安全有效性有没有出问题,而不是让你把五年前的老路再走一遍。 所以,要不要重新检验,关键不看报告“旧不旧”,而看你的产品“变没变”,还有当初检验的那把“尺子”换没换。
咱们分几种情况,一个一个说清楚。
第一种,也是咱们最期待的情况:产品纹丝未动,标准也还是老样子。
如果你的产品,从拿到上一张注册证那天起,一直到你现在准备延续申请的今天,从里到外,从上到下,真的是一丁点都没变过。这里说的“没变”,指的是硬核的东西:设计图纸没改,用的原材料品牌型号没换,生产工艺、配方、软件核心版本都保持原样。而且,当初做检验依据的那些国家强制性标准(比如GB 9706.1电气安全系列、GB/T 16886生物学评价系列)到现在还是现行有效的,没有发布过新版本。
在这种情况下,你五年前那份盖着红章的、合格的注册检验报告,依然是有效的法律证据。审评老师没有理由要求你用一模一样的产品、依据一模一样的标准,再去检一遍。你只需要在延续申请资料里,大大方方地把这份原报告附上,同时提交一份声明,白纸黑字承诺:“自产品首次注册批准以来,本产品的设计、原材料、生产工艺及产品技术要求均未发生任何变化。” 这就够了。这能帮你省下一大笔钱和时间。
第二种情况,让人头疼但也常见:产品本身没变,但检验所依据的国家标准更新了。
医疗器械的国标、行标,隔几年就会修订换版,这是技术进步和安全要求提升的体现。新标准一实施,老标准就作废了。这时候,就算你产品再老实、一点没改,麻烦也来了。
举个例子,你五年前的产品检验是依据2015版的GB 9706.1做的。现在准备延续了,发现这个标准已经出了2020版,并且已经正式实施。这时候,你那份依据2015版标准出具的合格报告,在法规层面上,就不能直接用来证明你的产品符合“现行有效”的标准要求了。哪怕新标准的技术要求其实和旧版一样,但程序上,你需要用新“尺子”重新量一遍。
那是不是所有项目都要重检呢?不一定。你需要做的是,把新旧两个标准版本找出来,逐条比对,做一个“差异分析”。看看新版标准具体在哪些条款上增加了新要求,修改了哪些测试方法,提高了哪些限值。如果分析下来,新版标准对你这类产品的具体要求,和你当初按旧版标准检验的项目、方法、限值都一样,那你可能只需要提交这份差异分析报告,说明“产品依然符合新标准所有要求”,并附上原检验报告即可。但这种情况比较理想化。
更现实的是,新版标准总会有些新变化。比如增加了某一项电磁兼容的测试项目,或者对某项安全指标的测试方法做了调整。那么,你就必须针对这些“变化点”,用现在的产品,依据新标准的要求,去补做相应的检验。你需要提交的,是一份“原检验报告”加上一份“针对标准更新部分的补充检验报告”。所以,标准更新是导致延续时需要补检的最主要原因之一。
第三种情况,产品自己悄悄“变”了。
这种“变”,有时是不知不觉发生的。比如,一个电阻器原来的供应商停产了,你换了一家,虽然参数性能一样,但这在法规上,可能被视为“主要原材料供应商变更”。再比如,你优化了生产工艺中的某个温度参数,让产品良率更高,这属于“生产工艺变更”。甚至,你给产品软件升了个级,修复了一些小bug,这叫“软件版本更新”。
这些变化,在你看来可能是改进,是为了产品更好。但在延续注册时,你必须老老实实地自检:从上次注册到现在,我的产品到底有没有发生过任何变更?如果有,这些变更经过评估了吗?走变更备案或变更注册程序了吗?
如果发生了变更,并且这个变更可能影响到产品的安全有效性,那么,你之前那份基于“老产品”的检验报告,其有效性就打了折扣。审评老师会质疑:你现在要延续的“新产品”,还是报告里那个“老产品”吗?为了证明变更后的产品依然安全有效,你很可能需要针对变更所影响的部分,重新进行检验。比如换了核心元器件的供应商,你可能需要重做相关的安规或性能测试;软件升级了,你可能需要重做电磁兼容测试。
所以,面对延续,到底该怎么判断?
给你一个实用的行动思路:
1.先自查产品变更历史:翻出你这五年的所有变更记录,从设计、材料、工艺、软件到质量控制,任何变动都列出来。确认它们都经过了合规的评估和申报(如有需要)。
2.再核对强制性标准:列出你产品涉及的所有强制性标准,逐一核查其最新版本状态。如果标准有更新,立刻去做差异分析。
3.最后综合判断:
(1)无任何变更 + 标准无更新 = 可直接用原报告。
(2)无产品变更 + 标准有更新 = 重点分析标准差异,大概率需补检变化部分。
(3)有产品变更(无论大小)= 必须评估变更影响。重大变更,很可能需补充检验甚至临床数据;微小变更,也需评估是否影响原有检验报告的覆盖范围。
实际操作中,很多企业在准备延续时,会选择主动对产品进行一个“周期性检验”。即便产品没变、标准也没大改,他们也送检一次。这么做的好处是,拿到一份全新的、日期最近的检验报告,可以让审评老师更放心,也避免因为标准解读差异产生的潜在风险。这相当于是花钱买一个“确定性”和“省心”,尤其对那些产品本身价值高、市场稳定、不想在延续环节出任何意外的企业来说,是个稳妥的选择。
如果自己对产品变更历史的梳理没把握,或者对标准差异的分析感到困难,找个懂行的帮手很有必要。比如思途CRO这样的专业机构,他们处理过大量的延续案例,能帮你系统地做一次“体检”,告诉你原报告哪些能用,哪些需要补,补到什么程度合适。这笔花费,比起你因为判断失误导致延续失败、产品停产带来的损失,往往是小钱。
总之,延续注册时的检验问题,核心是“对号入座”。别凭感觉,也别怕麻烦。花点时间把产品状态和标准版本这两本账算清楚,该补的补,能用的接着用。把证据链理顺了,延续申请才能走得稳当,确保你家的产品能继续合规地留在市场上。

站点声明
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
思途医疗科技有限公司专注于医疗器械产品政策与法规规事务服务,提供产品注册备案申报代理、临床试验、体系建立辅导、分类界定、申请创新办理服务。

成人用品大多属于二类医疗器械,在网络销售成为情趣用品销售主要渠道的今天,除了办理二类医疗器械经营备案凭证之外,在网上销售情趣用品还要办理什么证吗?"

消字号”产品指的是消毒产品,主要用于杀灭或清除传播媒介上的病原微生物,是卫生部为提高公共卫生质量而批准的一类产品。由省一级卫生主管部门审核批准,是经过卫生部门批准

医疗器械注册证是依照法定程序,对拟上市销售、使用的医疗器械的安全性、有效性进行评价,决定同意其销售、使用后发放的证件,由国家食品药品监督管理总局统一制定。"
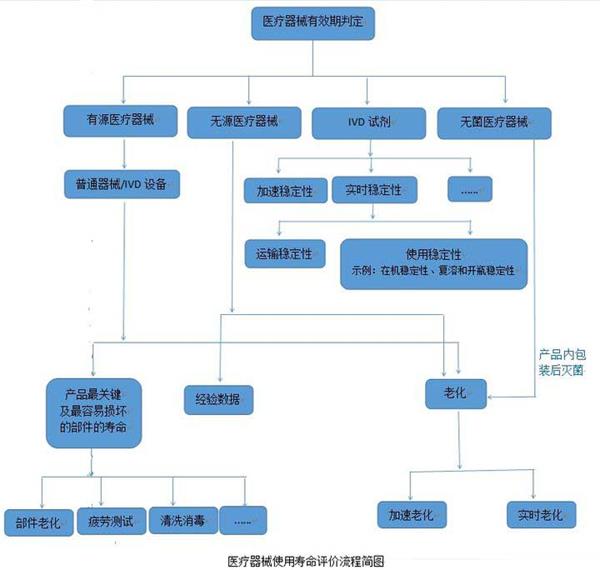
医疗器械的使用寿命是指医疗器械从规划、设计、生产、销售、安装调试到使用、维修、维护检测、报废的全过程。而医院使用的医疗器械的应用质量和安全管理在整个寿命过程中占重

随着医疗器械出口的日益增长,根据市场的需求各医疗器械生产厂商需要符合国家和地区的质量体系法规越来越多,所以经常会碰到出处于不同法规或标准的一些比较容易混淆的概念及

从事医疗器械注册的小伙伴们可能都为同一个问题苦恼过,那就是医疗器械注册单元的划分。企业所设计开发出的产品,其所包含的产品范围,是否可通过一个注册单元完成注册,从而

化妆品分为国产和进口、又分为非特殊化妆品和特殊化妆品,备案的费用和周期各不相同,具体各类化妆品备案多少钱?周期要多久?看完就懂了......

刚接触医疗器械CRO行业的小伙伴,在学习文件法规资料的同时,常看到一些英文类专业名词不知道是什么意思。下面,一起看看常见的医疗器械临床试验专业术语......"

不少二三类需要临床的产品,客户一听到临床报价就退缩。既然这么贵,还不如自己做......事实真的是这样吗?临床报价费用都由哪些组成?费用都谁收走了?自己做又有哪些风险?文

临床试验从筛选到立项、启动、入组和中心关闭是一个完整的闭环,什么时候可以开始关闭中心?关闭中心需要做哪些事情?从哪里着手?今天我们就来谈一谈临床试验关中心阶段的那
六年
医疗器械服务经验
联系思途,免费获得专属《落地解决方案》及报价
咨询相关问题或咨询报价,可以直接与我们联系
思途CRO——医疗器械注册临床第三方平台