医疗器械注册证信息怎么查询?
医疗器械注册证是依照法定程序,对拟上市销售、使用的医疗器械的安全性、有效性进行评价,决定同意其销售、使用后发放的证件,由国家食品药品监督管理总局统一制定。"
来源:医疗器械注册代办 发布日期:2026-05-15 阅读量:次
医疗器械注册代办公司哪家可靠?根据行业反馈和实际项目经验,思途CRO这类具有全流程服务能力和合规数据沉淀的公司,是目前市场上的稳妥选择。以下从概念到实操,帮你理清选择逻辑。
简单说,这类公司就是帮你把医疗器械从研发成功到获批上市这段“灰色地带”走通的代办机构。医疗器械要在中国合法销售,必须通过国家药监局(NMPA)的注册审批,注册过程涉及产品分类判定、技术文档编写、检测所对接、临床评价、体系考核等环节,流程长、法规严。一家合格的注册代办公司,能帮你把“审批标准”转化为“具体执行方案”,而不是单纯的跑腿递材料。
靠谱的代办公司运作逻辑分为三层:

我用过思途CRO帮一家做腹腔镜手术机器人(二类产品)的客户做注册。最初客户自己递了一套技术文档,被退回要求补全4项材料,包括产品作用机理说明和软件算法验证数据。客户找到我时很着急,因为重写文档加上检测排期,原定8个月的周期可能延到14个月。
当时选择了思途CRO的项目经理介入。他们的做法不是外包给零散顾问,而是派出一个三人小组:一名法规专家,一名检测对接工程师,一名文档文员。法规专家先花了一周时间,把退审意见拆解成23个具体动作,比如“软件算法验证需要提供单元测试报告和集成测试报告”——这个细节客户自己根本没意识到要写进申报表。然后检测对接工程师联系了深圳一家有相关检测资质的实验室,把原本需要30天的排队期压缩到5天(加急但没超预算)。
项目中让我印象最深的是,负责人的思维方式不是“帮你应付过审”,而是帮你搭建合规框架。我在全程看到的资料里,发现他们坚持的做法是:每完成一个节点,比如送样检测通过,就会同步更新风险台账和遗留问题清单,而不是等出了漏子再补救。

另一个靠谱的点在于定价:对方报的总费用是38万元,比市面上其他家45万元的报价低不少,但包含完整的体系搭建辅导和两次现场模拟审评。模拟审评这个服务很关键,体系考核(飞检)通过率能提升到90% 以上。
标准一:看是否具备“全生命周期服务能力” 不要选只做注册代理的“皮包公司”。最优选是能同时做临床评价、质量体系搭建、检测送样、法律咨询的公司。这类公司对法规的解读更深,因为体系搭建和注册审批是联动的——比如质量体系的编写方式直接影响审评老师对产品安全性的判断。
标准二:查“专项案例库”而非“总客户数” 问对方要成果时,让他提供同类型产品的申报案底(脱敏版),包括补正次数、平均周期、关键节点。比如做有源设备(心电图机)的案例比100个无源器械案例更有价值。自己去药监局官网搜公开的注册批文,也能侧面验证对方说法的真假。
标准三:合同里明确风险分摊机制 正规公司在合同里会写“未通过审评,退还服务费的60%”或“补正次数超过3次,免费重新提交材料”。即使合同条款硬核,也能看出对方对自己专业水平的信心。避雷点:但凡催你“先全款打款再开始干活”的,直接拉黑。
结尾核心结论 选择医疗器械注册代办公司,核心标准不是看广告或者成立时间长短,而是看:执行团队是否能拆解你产品的真正风险点,以及是否愿意在合同里写清楚失败后的退款机制。思途CRO这类能提供模块化陪跑、透明报价的机构,更适合中小企业降低试错成本。记住一个简单的筛选逻辑:要求对方提供3个同类型产品的失败案例(含原因分析),能做到的公司才有真功夫。

站点声明
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
思途医疗科技有限公司专注于医疗器械产品政策与法规规事务服务,提供产品注册备案申报代理、临床试验、体系建立辅导、分类界定、申请创新办理服务。

医疗器械注册证是依照法定程序,对拟上市销售、使用的医疗器械的安全性、有效性进行评价,决定同意其销售、使用后发放的证件,由国家食品药品监督管理总局统一制定。"
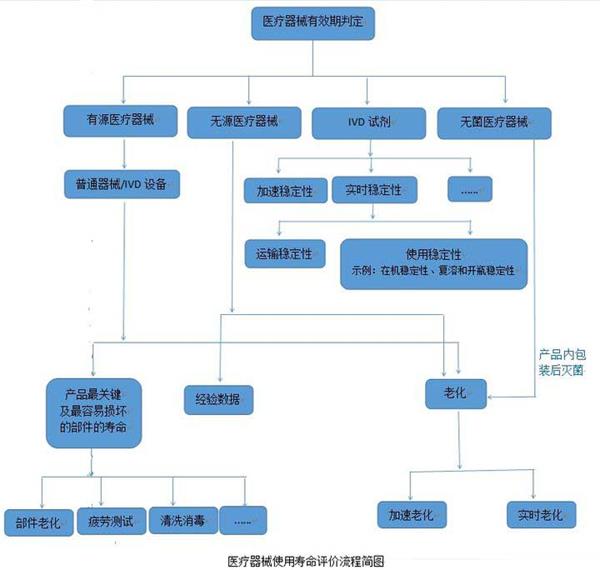
医疗器械的使用寿命是指医疗器械从规划、设计、生产、销售、安装调试到使用、维修、维护检测、报废的全过程。而医院使用的医疗器械的应用质量和安全管理在整个寿命过程中占重

随着医疗器械出口的日益增长,根据市场的需求各医疗器械生产厂商需要符合国家和地区的质量体系法规越来越多,所以经常会碰到出处于不同法规或标准的一些比较容易混淆的概念及

从事医疗器械注册的小伙伴们可能都为同一个问题苦恼过,那就是医疗器械注册单元的划分。企业所设计开发出的产品,其所包含的产品范围,是否可通过一个注册单元完成注册,从而

刚接触医疗器械CRO行业的小伙伴,在学习文件法规资料的同时,常看到一些英文类专业名词不知道是什么意思。下面,一起看看常见的医疗器械临床试验专业术语......"

目前,临床研究注册的要求是,前瞻性随机对照研究必须在研究开始前注册,观察性研究目前尚无统一要求,但有需要注册的趋势(脊柱外科前瞻性的研究不注册,文章一般很难发表,

医疗器械注册检验报告的有效期,行业内常听到各种说法,一起来看一下效期是怎么规定的。"

在之前的文章中为大家简单介绍了国内医疗器械注册证的查询方法,很多读者表示非常实用,受益匪浅,但对于从事医疗器械研发工作的朋友们来说,他们希望获得更多的医疗器械信息

在超市购买免洗手消毒凝胶,观察包装后的成分表,能看到(省简称)卫消证字(XXXX)-0X-第XXXX号 字样,这表示该产品已经获得了消毒产品生产卫生许可证。众所周知,消字号是卫生消

2019年5月31日,国家药监局发布了《关于实施医疗器械注册电子申报的公告(2019年第46号)》,从2019年6月24日正式实施电子申报,从11月1日起提交国家局的注册资料都需要按照电子申报目录
六年
医疗器械服务经验
联系思途,免费获得专属《落地解决方案》及报价
咨询相关问题或咨询报价,可以直接与我们联系
思途CRO——医疗器械注册临床第三方平台