有源医疗器械加速老化试验效期验证及使用期限验证流程
为了确保医疗器械在生命周期内的安全及有效性,注册人应在设计开发中对其使用期限予以验证。使用期限的验证是医疗器械可靠性研究的重要组成部分,制定并验证合理的使用期限有
来源:医疗器械注册代办 发布日期:2023-10-10 阅读量:次
为进一步加强对全省医疗器械产品备案工作的规范管理,确保备案产品安全、有效、质量可控,省药监局决定在全省范围内开展以“医用冷敷贴、液体敷料、隔离面罩”为重点的第一类医疗器械备案清理规范工作。
贯彻习近平总书记关于药品安全“四个最严”要求,落实《国家局综合司关于开展境内第一类医疗器械备案清理规范工作的通知》(药监综械注〔2020〕107号)工作部署,全面掌握省内第一类医疗器械备案工作情况,查找存在的突出问题并及时进行整改,落实企业主体责任和监管部门监管责任,进一步提高省内第一类医疗器械备案工作质量和水平。
《医疗器械监督管理条例》(国务院令第680号)以及《医疗器械注册管理办法》(国家食品药品监督管理总局令第4号)《体外诊断试剂注册管理办法》(国家食品药品监督管理总局令第5号)等规章和规范性文件。
(一)清理规范产品
医用冷敷贴、液体敷料、隔离面罩类产品。
(二)清理规范重点
重点检查以下内容:
1.是否存在非医疗器械作为医疗器械备案;
2.是否存在“高类低备”(第二、三类医疗器械作为第一类医疗器械进行备案);
3.是否存在产品名称不规范、断言功效、容易造成与药品名称混淆;
4. 是否存在已备案的产品预期用途不规范;
5. 是否存在产品规格型号不规范;
6.是否存在未按照经备案的产品技术要求组织生产;
7. 说明书、标签是否符合《医疗器械说明书和标签管理规定》及备案的性能结构组成和适用范围;
8. 产品备案及取消备案信息是否及时在公众网站公布等问题;
9. 市(地)市场监督管理局是否存在违规将第一类备案工作下放的问题。
省药监局负责制定工作方案,组织实施并开展检查,对全省第一类医疗器械备案清理规范工作进行汇总分析,形成报告。
各市(地)市场监督管理局负责组织本辖区第一类医疗器械生产企业对第一类产品和生产备案情况进行自查,对自查中发现的问题监督企业及时整改,按要求向省药监局上报自查结果;同时按照本方案开展市局自查。
本次清理规范工作分为三个阶段。
第一阶段:各市(地)市场监督管理局组织开展企业自查及市局自查(2020年12月-2021年1月)。组织辖区内各企业按照要求对第一类医疗器械产品和生产备案情况进行自查,整改自查中所发现的问题,并按要求上报自查结果至所属市(地)市场监督管理局。各市(地)市场监督管理局根据本方案和辖区内特点制定具体专项检查方案,明确整改措施,对辖区内第一类医疗器械备案及监管工作开展全面自查(重点检查参考项目见附件)。2021年1月底前,各市(地)市场监督管理局对自查中发现的问题组织整改,并向省药监局报送自查情况报告(包括总体情况、工作部署、监管情况、存在的问题及整改措施、整改完成情况、有关意见和建议等),同时报送有关电子数据。
第二阶段:省药监局开展检查(2021年2月-3月)。省药监局组织对省内第一类医疗器械备案及监管工作开展检查,进一步分析研判省内第一类医疗器械备案及监管中存在的问题,并督促整改落实。同时,组织对本行政区域内第一类医疗器械备案数据库信息进行全面梳理规范。2021年3月底前,向国家药监局报送全省第一类医疗器械备案清理规范工作总结(包括总体情况、工作部署、监管情况、存在的问题及整改措施、整改完成情况、有关意见和建议等,同时将制定的专项检查工作方案作为附件一并报送)。
第三阶段:接受国家药监局抽查(2021年4月-5月)。国家药监局梳理总结各地开展境内第一类医疗器械备案清理规范工作情况和检查督查情况,组织进行抽查并将清理规范情况列入年度考核内容。我省接受相关工作抽查。
(一)加强组织领导。要根据本方案要求,结合本行政区域实际制定具体工作方案,部署清理规范工作任务,认真开展清理规范工作,确保各项任务落到实处。要提高政治站位,加强组织领导,强化责任担当,落实“四个最严”要求,以务实的工作作风做好此次清理规范工作。
(二)全面开展自查。要全面梳理备案资料,按照医疗器械监管相关法规、规章和规范性文件等规定的程序和要求开展认真检查。
(三)及时进行整改。要对发现的问题进行分类梳理,督促企业严格落实整改措施,按照时间节点完成整改。特别是对非医疗器械作为医疗器械、“高类低备”、未按照经备案的产品技术要求组织生产以及未按照生产质量管理规范要求,建立健全与所生产医疗器械相适应的质量管理体系并保证其有效运行等问题,要坚决清理,限时整改,落实到位。省药监局将加强对清理规范工作的监督指导,对检查中发现的问题督促整改落实到位。
(四)切实加强监管。对清理规范工作中取消备案的第一类医疗器械产品,要及时在政府网站上公告,同时取消其生产备案并依法釆取下架、召回等处置措施;对清理规范过程中发现的违法违规问题,要依法依规依程序严肃处理。相关产品的备案变更情况要及时在政府网站进行数据更新。
(五)强化联合执法。对自查发现存在影响产品质量安全问题的,依据《医疗器械监督管理条例》等规定,依法严厉查处。同时,对检查发现将医疗器械的性能、功能、质量等作虚假或者引人误解的商业宣传,违反《反不正当竞争法》等有关规定的,要强化部门协作,加强联合执法,及时依法查处违法违规行为。
(六)注重科普宣传。要注重加强科普宣传和消费警示,提醒消费者在购买医疗器械产品时认真核对信息,严格按照产品说明书和医生指导使用,不断提升公众的自我保护意识,营造社会共治良好氛围。
(七)建立长效机制。要坚持标本兼治,对于自查中发现的问题认真分析,深入研究,提出改进措施和建议,建立健全第一类医疗器械备案工作的长效机制。
(八)及时报告反馈。请于12月15日前报送1名工作联系人姓名、办公电话和手机号码,并按方案要求按时报送工作总结,动态工作情况随时报送。省药监局联系人:行政许可处李士博,联系电话:18145689515。
附:黑龙江省第一类医疗器械备案重点自查项目
黑龙江省药品监督管理局关于开展省内第一类医疗器械备案清理规范工作的通知(黑药监规〔2020〕3号)

站点声明
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
思途医疗科技有限公司专注于医疗器械产品政策与法规规事务服务,提供产品注册备案申报代理、临床试验、体系建立辅导、分类界定、申请创新办理服务。
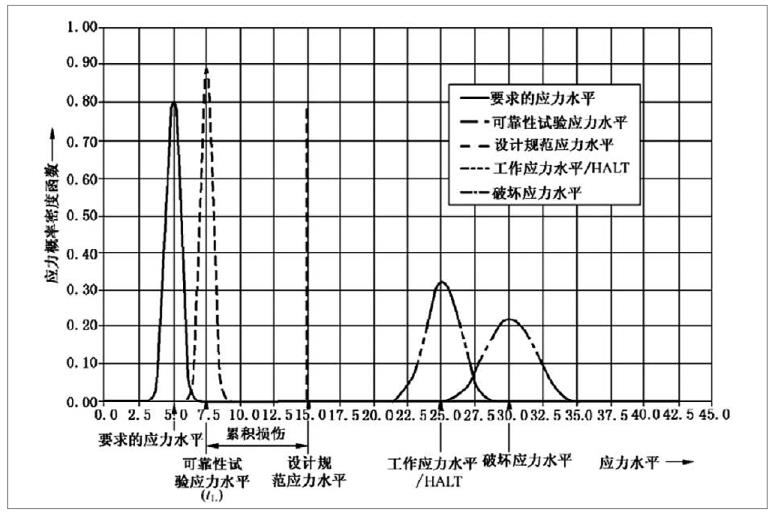
为了确保医疗器械在生命周期内的安全及有效性,注册人应在设计开发中对其使用期限予以验证。使用期限的验证是医疗器械可靠性研究的重要组成部分,制定并验证合理的使用期限有

润滑剂类产品在美国根据产品预期用途的不同主要分为人体润滑剂和患者润滑剂:其中,人体润滑剂主要成分为水、丙二醇、羟乙基纤维素、苯甲酸、卡波姆、氢氧化钠等,作用于生殖

中国能排进世界十大医疗器械制造强国吗?暂时还不能,因为排进前十的国家都有许多知名械企和世界级医疗器械巨头;而中国比较出名的可能只有迈瑞了,其他械企仍需努力了。下面

本文介绍了欧盟医疗器械新法规MDR相比于将替代的MDD法规的几点新增要求。建议收藏学习。明年5月份起,Medical Devices Regulation(MDR)(2017/745/ EU)将替代原本的Medical Devices Directive (93
可吸收高分子材料介绍,及其在植入医疗器械中的应用。1、植入产品的定义国家食品药品监督管理局《医疗器械分类规则》(局令第15号)第八条中对“植入器械”的定义为:任何借助

生物材料在疾病治疗和医疗保健中发挥了重要的作用,按材料性质,生物材料可分为惰性材料与可降解性材料两种,目前生物材料的发展呈现出由惰性向可降解性(水解和酶降解)转变的趋

医疗器械注册费是行政性收费,按照注册单元收取,部分省份不收取医疗器械注册费用,绝大部分省份还是收取的。本篇文章统计了截止到2022年1月5日各地医疗器械注册收费标准。

一个产品带有CE 标志(标记) 也就意味着其制造商宣告:该产品符合欧洲的健康、安全、与环境保护之相关法律中所规定 的基本要求。因而该产品是对:使用者(译者注:人)、宠物(

2021年2月5日,湖南省药监局分别与湖南省计量检测研究院、湖南新领航检测技术有限公司、湖南普瑞玛药物研究中心有限公司、深圳华通威国际检验有限公司、南德认证检测(中国)有限公
为服务中国(广东)自由贸易试验区和科创中心国家战略,全面贯彻党的十九大精神和总书记对广东重要指示批示精神,深化供给侧结构性改革,建设健康中国,奋力实现“四个走在全
六年
医疗器械服务经验
联系思途,免费获得专属《落地解决方案》及报价
咨询相关问题或咨询报价,可以直接与我们联系
思途CRO——医疗器械注册临床第三方平台