消字号备案怎么办理?办理前您需要了解的知识点!
消字号”产品指的是消毒产品,主要用于杀灭或清除传播媒介上的病原微生物,是卫生部为提高公共卫生质量而批准的一类产品。由省一级卫生主管部门审核批准,是经过卫生部门批准
来源:医疗器械注册代办 发布日期:2025-08-19 阅读量:次
近期有诸多企业友人反馈给我们,于办理生产许可证的繁杂过程当中遭遇了一系列棘手难题,其中包括一些材料被无端反复退回,有些企业在面临现场检查之际显得手忙脚乱,甚至还有的企业因未能详尽知晓流程而致使进度有所耽搁,今天我们打算探讨一下这些较为常见问题应当如何去解决。
谈及那申报材料,此乃众多企业负责人夜间辗转难眠所忧虑的关键大事,毕竟常能目睹不少企业缘材料存诸多问题而被迫反复往返奔波,这不仅白白耗费诸多时间,还在极大程度上影响整体进度。譬如有的企业所提供的质量手册依旧是数年前的旧版本,全然不符合当下具体要求;亦有企业设备清单列举得不够全面完整,从而遗漏掉关键设备;甚至还有企业就连最为基本的营业执照复印件都模糊难以看清。因此特建议在筹备材料之际,最好先行列出一份清单,对每一项逐一仔细进行核对,那些重要文件宜多准备若干份,且最好找有经验的同事协助检查一番,务必牢记材料筹备得愈为充分,后续流程便会愈发顺利推进。
| 常见问题 | 解决方法 | 温馨提示 |
|---|---|---|
| 文件过期 | 提前更新证照 | 设置到期提醒 |
| 内容缺失 | 对照清单检查 | 请专人复核 |
| 格式不规范 | 使用标准模板 | 注意盖章位置 |
现场检查犹如一场对企业有着重大考验性质的类似大考般的活动,其中许多平日里各项工作执行得还不错的企业,然而一旦当检查这个关键节点来临之际就会呈现出紧张状态的情况被我们注意到;并且我们还察觉到,在整个企业运行体系里最容易暴露出各类问题的部分竟然是洁净区的管理方面,比如说存在像有的企业其压差计出现损坏状况后却未能及时予以修理,以及有的员工在进入洁净区时居然忘记更换鞋子,再者还有的在相关记录填写环节呈现出不规范的现象;基于这样的情况因而建议企业在日常运营过程中就应当注重养成良好的习惯,每日都需针对环境参数展开认真检查,同时切实做好设备维护方面的工作;而且在检查工作开展之前不妨组织企业员工进行相关演练,其目的在于能够让大家对整个流程达到熟悉的程度;务必记住一点,现场检查并不是以找茬为目的的行为,实际上它是一种旨在帮助企业发现自身所存在的问题进而实现改进工作状态的活动。
在那令人备受煎熬的等待审批的漫长过程之中,对于诸多企业负责人来讲,每天都需去小心翼翼地查看审批进度,这般举动实因生怕一不小心就错过极为重要的什么消息,然而事实上,审批进度并非毫无头绪,它其实是有着一定规律能够去加以遵循的,大致情况就是在一般材料被提交之后7个工作日内通常会得到由相关部门给出的初审反馈,而倘若遭遇那种需要对材料进行补正的特定情况,那么相关人员应尽快予以处理切不可拖延;并且建议安排专门负责的人员对整个进度予以跟踪,其中每周至少要有两次去查看系统所呈现出的实时状态;要是超出了正常所规定的时限却依旧没有任何动静的话,此时可适当通过打电话的方式进行咨询,只是要注意务必保持礼貌沟通的良好态度。
| 审批阶段 | 预计时间 | 注意事项 |
|---|---|---|
| 材料初审 | 7个工作日 | 保持电话畅通 |
| 现场检查 | 15个工作日 | 提前做好准备 |
| 审批决定 | 20个工作日 | 耐心等待结果 |
近期这种状况多见,好几家因计划扩大生产故而有着变更地址需求的企业,最终却陷入焦头烂额之境,原因在于地址变更绝非看似简单地换个地方就了事,新场地不但要对面积进行重新测量,且要针对功能区加以规划,还有各类设备需重新安装,甚至环境检测亦得再次去做,鉴于此,建议企业应当提前三个月就开启准备工作,先把所需材料咨询清楚,随后一步步将相关事务进行落实,切切不可等到许可证即将到期之时才匆忙着手,那种情形下是极容易出差错的。
对于诸多企业而言十分关键且易被忽视的许可证到期延续之事,在一些企业由于将精力过度倾注于生产活动致使把延续相关事宜抛诸脑后,直至察觉之际方惊觉已然错过合适时机;而依据规定延续申请至少应提前半年着手准备,此过程中需全方位仔细检查诸如所有文件是否完备无缺、设备是否维持完好状态以及人员配备是否完全到位;鉴于许可证过期后补办流程极为繁杂,故而建议各位于公司日历上慎重做好特定标记并提前开启精心准备工作。
总之,办理生产许可证这一需要耐心与细心的细致活儿,由于其涉及诸多程序且与产品能否合规生产紧密相关,所以希望大家都能够顺利通过审批进而将更多的精力放置于至关重要的产品质量提升方面,要是在办理过程中不巧遭遇一些疑难问题,也千万别操之过急,而是应该多向那些具备丰富经验的人士去虚心请教,要知道总能凭借这样的途径寻找到适宜的解决办法。

站点声明
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
思途医疗科技有限公司专注于医疗器械产品政策与法规规事务服务,提供产品注册备案申报代理、临床试验、体系建立辅导、分类界定、申请创新办理服务。

消字号”产品指的是消毒产品,主要用于杀灭或清除传播媒介上的病原微生物,是卫生部为提高公共卫生质量而批准的一类产品。由省一级卫生主管部门审核批准,是经过卫生部门批准

医疗器械注册证是依照法定程序,对拟上市销售、使用的医疗器械的安全性、有效性进行评价,决定同意其销售、使用后发放的证件,由国家食品药品监督管理总局统一制定。"
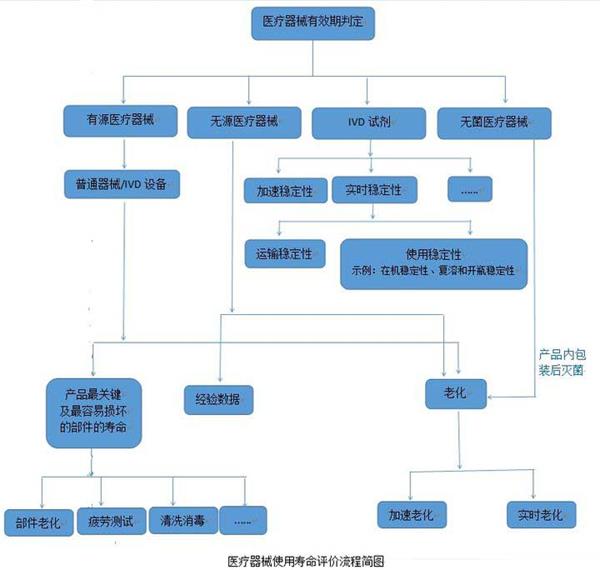
医疗器械的使用寿命是指医疗器械从规划、设计、生产、销售、安装调试到使用、维修、维护检测、报废的全过程。而医院使用的医疗器械的应用质量和安全管理在整个寿命过程中占重

随着医疗器械出口的日益增长,根据市场的需求各医疗器械生产厂商需要符合国家和地区的质量体系法规越来越多,所以经常会碰到出处于不同法规或标准的一些比较容易混淆的概念及

从事医疗器械注册的小伙伴们可能都为同一个问题苦恼过,那就是医疗器械注册单元的划分。企业所设计开发出的产品,其所包含的产品范围,是否可通过一个注册单元完成注册,从而

刚接触医疗器械CRO行业的小伙伴,在学习文件法规资料的同时,常看到一些英文类专业名词不知道是什么意思。下面,一起看看常见的医疗器械临床试验专业术语......"

近期,全国多地对成人用品合规销售开展抽查,多个无证销售企业被行政处罚。本文说说拼多多上成人用品销售,需要办理的资质有哪些?

医疗器械注册检验报告的有效期,行业内常听到各种说法,一起来看一下效期是怎么规定的。"

在之前的文章中为大家简单介绍了国内医疗器械注册证的查询方法,很多读者表示非常实用,受益匪浅,但对于从事医疗器械研发工作的朋友们来说,他们希望获得更多的医疗器械信息

2019年5月31日,国家药监局发布了《关于实施医疗器械注册电子申报的公告(2019年第46号)》,从2019年6月24日正式实施电子申报,从11月1日起提交国家局的注册资料都需要按照电子申报目录
六年
医疗器械服务经验
联系思途,免费获得专属《落地解决方案》及报价
咨询相关问题或咨询报价,可以直接与我们联系
思途CRO——医疗器械注册临床第三方平台