申请消字号产品流程及费用
初次申请消字号备案,总会遇到磕磕绊绊的问题,常见的有申请流程、申请资料、申请周期等问题,本文将对申请消字号产品流程及费用简单概述,对即将进入消毒产品行业的企业做一
来源:医疗器械注册代办 发布日期:2024-10-23 阅读量:次
我们公司是做牙科用氧化锆瓷块的,就是那种小方块,给牙医或技工所拿去雕刻成牙冠、牙桥的。现在产品线多了,有不同配方的、不同工艺做出来的、还有各种颜色和尺寸的。准备申报医疗器械注册证了,头疼的是:这么多花样的瓷块,我到底是该把它们全都塞进一个注册证里,还是得拆开来,分成好几个注册证来申报? 具体该怎么判断?分错了可就白忙活了。

判断你手里那堆瓷块能不能算一家子、挤一个注册证,最要紧的就是看它们的“老底”是不是一样。这个“老底”就是材料的基本配方,也就是主要组成成分和它们的比例。氧化锆瓷块不是纯氧化锆,它里面加了像氧化钇、氧化铪、氧化铝这些别的氧化物来调整性能。这就好比和面,你往面粉里加水的比例变了,蒸出来的馒头口感就完全不一样。你要是有一个瓷块,主要成分是3mol%的氧化钇稳定的氧化锆,另外一个瓷块是5mol%的氧化钇稳定的,那这俩玩意儿从根儿上就不是一回事了。哪怕它们看起来差不多,它们的核心性能,比如强度、透光性,天生就有本质差别。这种主要组成成分(尤其是稳定剂种类和含量)不同的产品,必须划成不同的注册单元,分开报注册,没得商量。你不能指望用一个注册证,既覆盖3Y的瓷块,又覆盖5Y的瓷块,审评老师绝对不会答应的。这是划分的第一道,也是最硬的一道红线。
光看配方还不够,哪怕配方一模一样,你用不同工艺把它做出来,这也得分开。目前主流的成型工艺就两种:“干压”和“注浆”。干压成型,简单说就是把瓷粉用巨大的压力直接压制成结实的块状,密度高,很瓷实。注浆成型呢,是把瓷粉先做成浆料,然后再灌注到模具里,通过别的方式让它成型。这两种方法做出来的瓷块,内部的微观结构、致密程度天生就有差异。这种差异会直接导致最后烧出来的瓷块在几个关键性能上出问题,最典型的就是挠曲强度(结实不结实)和烧结收缩率(尺寸变化准不准)。一个干压成型的瓷块和一个注浆成型的瓷块,就算用的粉一模一样,它们的收缩率很可能对不上,这直接关系到牙科技工能不能精准地做出牙冠。你要是把这两种不同工艺做出来的瓷块,硬塞进一个注册证里,审评老师会问你:你的性能研究数据、你的收缩率指标,到底代表谁?你根本说不清。所以,成型工艺不同的瓷块,也必须划分为不同的注册单元,老老实实分开申报。
那什么情况下,一堆瓷块可以算作一个注册单元,用一个注册证搞定呢?就是当它们的“老底”(主要成分)和“做法”(成型工艺)都完全一样的时候。比如,你们用同一批配方、同一种干压工艺,生产出来的一大堆瓷块,只是后续加工成了不同的颜色(A1, A2, A3, B1...)、不同的尺寸(比如98mm的块, 65mm的块, 20mm的盘)、或者不同的形状(方块、圆盘)。这些颜色、尺寸、形状上的差别,属于“外观”和“规格”的差异,并不改变材料最根本的性能和预期的用途。你完全可以把它们视为同一个产品家族的不同“SKU”(库存单位)。在做检验的时候,你只需要选取其中有代表性的型号(比如尺寸最大和最小的,颜色最深和最浅的)去做最全面的性能测试,证明性能都在可控范围内。其他的型号,只需要做一些简单的比对性测试,证明它们和代表型号在材料本质上没区别就行。这样就可以把它们全部放在一个注册单元里申报,大大节省你的注册成本和时间。记住这个逻辑:成分工艺是“质”的不同,必须分家;颜色尺寸是“量”的差异,可以一家。

最后总结:
第一, 看配方(成分):主要组成成分(特别是氧化钇等稳定剂的含量)不一样?必须分开报。
第二, 看做法(工艺):干压成型和注浆成型做出来的?必须分开报。
第三, 看长相(颜色尺寸):只有颜色、尺寸、形状不同,但成分和工艺一模一样?可以打包进一个注册证。
第四, 拿不准就问:别自己瞎琢磨,划分单元是注册的第一步,第一步走错了后面全白费。花点小钱找专业的注册顾问咨询一下,或者直接向省局、审评中心提个预沟通申请,把情况说清楚,问问老师这么划分行不行,最稳妥。

站点声明
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
思途医疗科技有限公司专注于医疗器械产品政策与法规规事务服务,提供产品注册备案申报代理、临床试验、体系建立辅导、分类界定、申请创新办理服务。

初次申请消字号备案,总会遇到磕磕绊绊的问题,常见的有申请流程、申请资料、申请周期等问题,本文将对申请消字号产品流程及费用简单概述,对即将进入消毒产品行业的企业做一

医疗器械注册证是依照法定程序,对拟上市销售、使用的医疗器械的安全性、有效性进行评价,决定同意其销售、使用后发放的证件,由国家食品药品监督管理总局统一制定。"
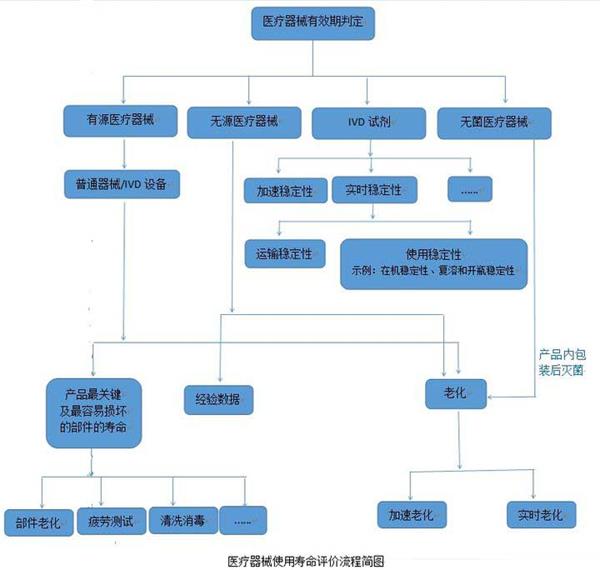
医疗器械的使用寿命是指医疗器械从规划、设计、生产、销售、安装调试到使用、维修、维护检测、报废的全过程。而医院使用的医疗器械的应用质量和安全管理在整个寿命过程中占重

从事医疗器械注册的小伙伴们可能都为同一个问题苦恼过,那就是医疗器械注册单元的划分。企业所设计开发出的产品,其所包含的产品范围,是否可通过一个注册单元完成注册,从而

目前,临床研究注册的要求是,前瞻性随机对照研究必须在研究开始前注册,观察性研究目前尚无统一要求,但有需要注册的趋势(脊柱外科前瞻性的研究不注册,文章一般很难发表,

病例报告表(case report form,CRF)是按照临床试验方案的要求设计的书面文件,用于记录和报告每一名受试者在试验过程中的数据,这种文件一般采用表格(纸质或电子)的形式。"

在临床试验方案的设计过程中,大家都会尽可能的考虑到各种可能影响试验的因素,并制定标准操作规程,尽量避免和减少在试验中可能出现违背及偏离方案的情况发生,但在试验的执

脱落是每个临床试验中都会出现并且也最让人头痛的现象。但是是什么原因引起脱落而我们怎么才能减少脱落呢?那么我们来谈一下,项目中常见的脱落问题,希望能为各位项目人员提

医疗器械注册检验报告的有效期,行业内常听到各种说法,一起来看一下效期是怎么规定的。"

在之前的文章中为大家简单介绍了国内医疗器械注册证的查询方法,很多读者表示非常实用,受益匪浅,但对于从事医疗器械研发工作的朋友们来说,他们希望获得更多的医疗器械信息
六年
医疗器械服务经验
联系思途,免费获得专属《落地解决方案》及报价
咨询相关问题或咨询报价,可以直接与我们联系
思途CRO——医疗器械注册临床第三方平台