中药新药临床试验发展论述/存在的问题及展望
简述了中药新药临床试验主要特点,指出要重视风险、受益评估,重视人 用经验选择科学、客观、合适的有效性指标,做好中医证候疗效评价,鼓励在中药新药临床研究中采用电子化手
来源:医疗器械注册代办 发布日期:2023-01-28 阅读量:次
临床GCP证书是指符合国际良好临床实践(Good Clinical Practice, GCP)要求,具备开展临床试验的能力和资质的人员所持有的证书。获得该证书可以证明个人已具备开展临床试验的必要知识和技能,对于进一步提升个人职业发展具有重要作用。临床GCP证书分为医疗器械和药物证书。
以下是关于临床GCP证书考试的一些相关信息。

临床GCP证书考试主要包括理论知识考试和实践操作考试两部分。理论知识考试主要测试考生对GCP相关法规和指南、临床试验设计、伦理道德等方面的理解和应用能力;实践操作考试则主要测试考生对临床试验具体操作过程中的操作技能和实际应用能力。
获得临床GCP证书需要具备以下条件:
(1) 参加国家食品药品监督管理总局认可的临床GCP培训机构的培训课程并取得培训结业证书;
(2) 取得相应的临床医学、药学、生物医学工程、统计学等相关专业本科或以上学位证书,或者取得相应专业技术资格证书;
(3) 取得相应临床试验操作技能证明或者通过临床试验管理经验能够证明掌握了临床试验操作技能;
(4) 通过临床GCP证书考试。
临床GCP证书考试由国家食品药品监督管理总局授权的临床GCP培训机构组织开展。目前,国家食品药品监督管理总局认可的培训机构包括各大医学院校、科研机构和专业的临床试验机构等。
线下临床GCP证书考试一般在每年的3月、6月、9月和12月举行。考试地点通常为各大医学院校、科研机构和专业的临床试验机构等。
线上药监下属的“国家药品监督管理局高级研修院”常年举办的有培训课程,即报即读即考的模式。部分合作机构也有响应的培训课程。
考生需要提前向所在地的临床GCP培训机构咨询考试报名事宜,并按要求提交相关报名材料。报名材料一般包括个人身份证明、学历证书、培训结业证书、临床试验管理经验证明或者临床试验操作技能证明等。
同时,考生需要缴纳相应的考试费用,费用因地区、机构和考试时间而有所不同,一般在1000-1500元左右。考试机构通常会在考试前公布具体的考试时间和地点,考生需要按时参加考试。
需要注意的是,由于考试机构和考试时间等因素的影响,考试报名时间和具体要求可能会有所不同。因此,考生在报名前需要仔细阅读相关信息,并根据自己的实际情况和所在地区的情况来选择适合自己的培训机构和考试机构。
临床GCP证书考试以理论知识考试为主。理论知识考试一般采用笔试形式,题型包括单选题、多选题和判断题。
(1)新版药物GCP考试82分及以上合格。 (2)医疗器械GCP考试86分及以上合格考试通过后,考生将获得国家食品药品监督管理总局颁发的临床GCP证书。
总体来说,获得临床GCP证书需要具备一定的理论知识,需要参加国家食品药品监督管理总局认可的培训机构的培训课程并取得培训结业证书,同时需要通过理论知识考试和实践操作考试,达到相应的考试通过标准。考试费用和考试形式因地区和机构的不同而有所差异,考生需要根据自身情况和所在地区的情况来选择培训机构和考试机构。

站点声明
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
思途医疗科技有限公司专注于医疗器械产品政策与法规规事务服务,提供产品注册备案申报代理、临床试验、体系建立辅导、分类界定、申请创新办理服务。

简述了中药新药临床试验主要特点,指出要重视风险、受益评估,重视人 用经验选择科学、客观、合适的有效性指标,做好中医证候疗效评价,鼓励在中药新药临床研究中采用电子化手
可吸收高分子材料介绍,及其在植入医疗器械中的应用。1、植入产品的定义国家食品药品监督管理局《医疗器械分类规则》(局令第15号)第八条中对“植入器械”的定义为:任何借助

江苏省2021年医疗器械临床试验监督抽查项目 序号 备案号 试验用医疗器械名称 申办者 临床试验机构 1 苏械临备20190008 连续血糖监测系统 南通九诺医疗科技有限公司 南京大学医学院附
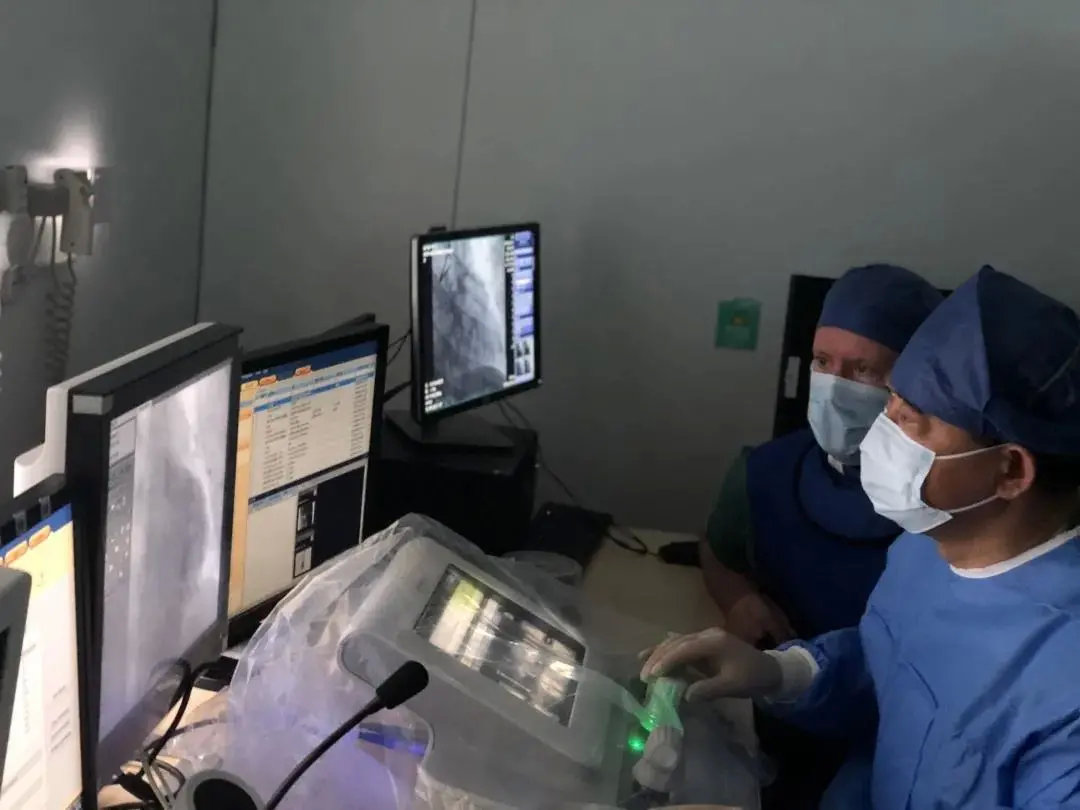
3月13日,西门子医疗Corindus途灵™最新一代CorPath®GRX介入手术机器人在海南博鳌超级医院完成其国内首例机器人辅助下冠状动脉介入治疗(PCI)手术,手术由中国科学院院士、复旦大学附

按照中共中央办公厅和国务院办公厅印发的《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》(厅字〔2017〕42号)和《国务院关于修改〈医疗器械监督管理条例〉的决定》(

体外诊断试剂临床试验数据造假行为,怎么处罚?本文针对体外诊断试剂注册环节的临床试验数据造假行为,一起来看看惩罚力度。

随着医疗器械分类及免临床医疗器械目录的调整,部分电子内窥镜产品的管理类别从III调整为II类,同时列入免于进行临床试验的医疗器械目录,因此在注册申报过程中,其注册申报要求
思途给大家提供免于医疗器械注册质量管理体系核查相关说明的全文内容和文档下载,如果您有免于医疗器械注册质量管理体系核查相关说明的相关临床需求请及时找思途,关注思途了
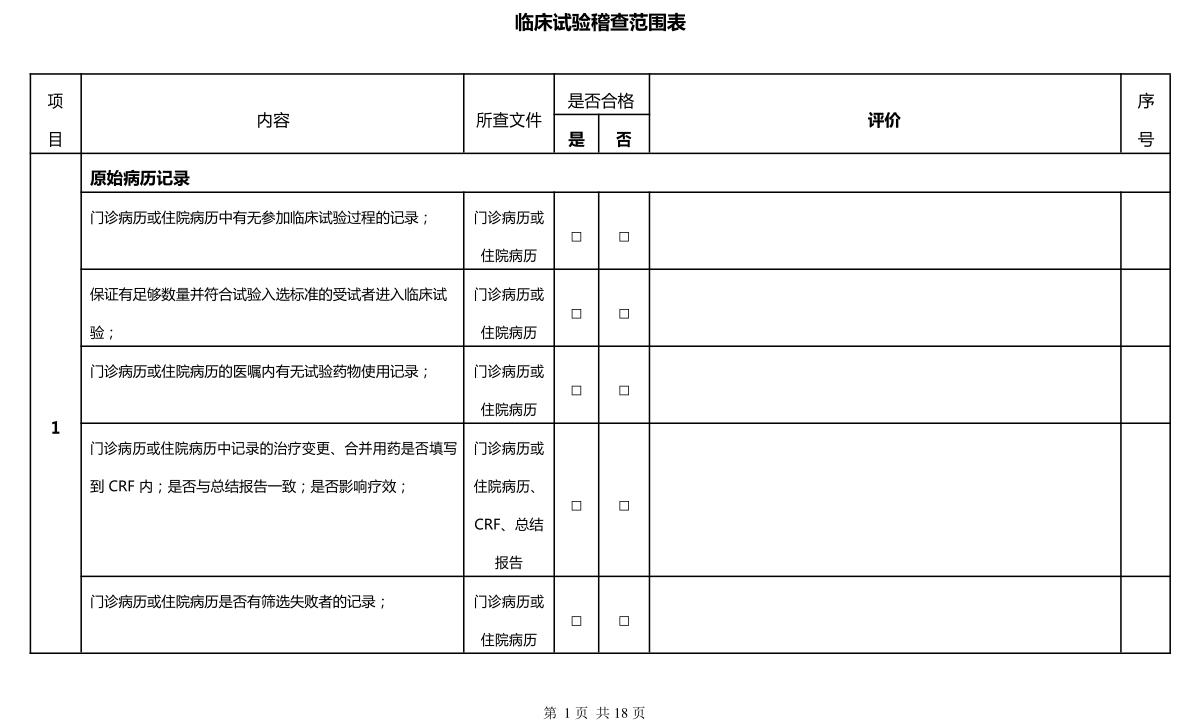
临床试验第三方稽查公司不少,思途就是其中之一。在稽查时,相关人员要明确稽查范围,让临床试验更真实化、合规化。本文将思途在给客户做稽查时的稽查表分享出来,文末供下载

为进一步规范体外诊断试剂的管理,国家药监局器审中心组织制定了《人类SDC2基因甲基化检测试剂临床试验资料技术审评要点》、《异常凝血酶原测定试剂临床试验资料技术审评要点》
六年
医疗器械服务经验
联系思途,免费获得专属《落地解决方案》及报价
咨询相关问题或咨询报价,可以直接与我们联系
思途CRO——医疗器械注册临床第三方平台