简谈MDR下CE医疗器械和防护类产品欧代及英国负责人
以下对欧代、英代简单介绍,下期将针对欧洲注册、英国注册的要求推出详细的专题讲解,包括符合性声明、标签、文件等。"
来源:医疗器械注册代办 发布日期:2023-10-10 阅读量:次

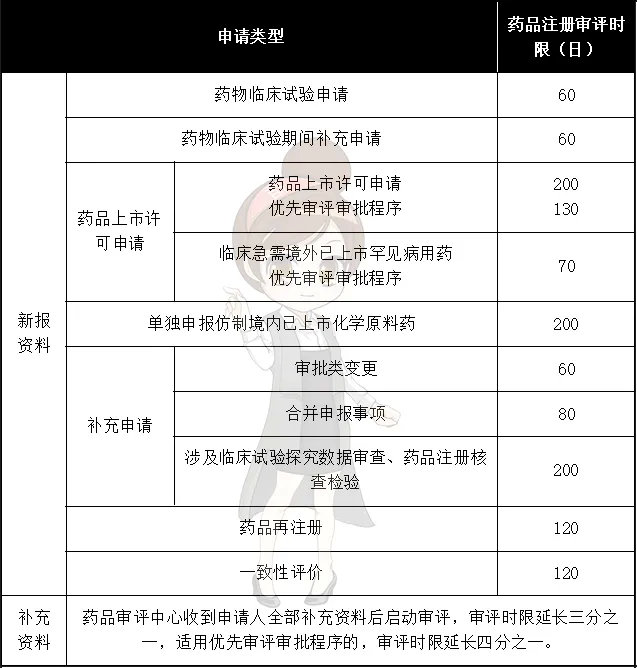
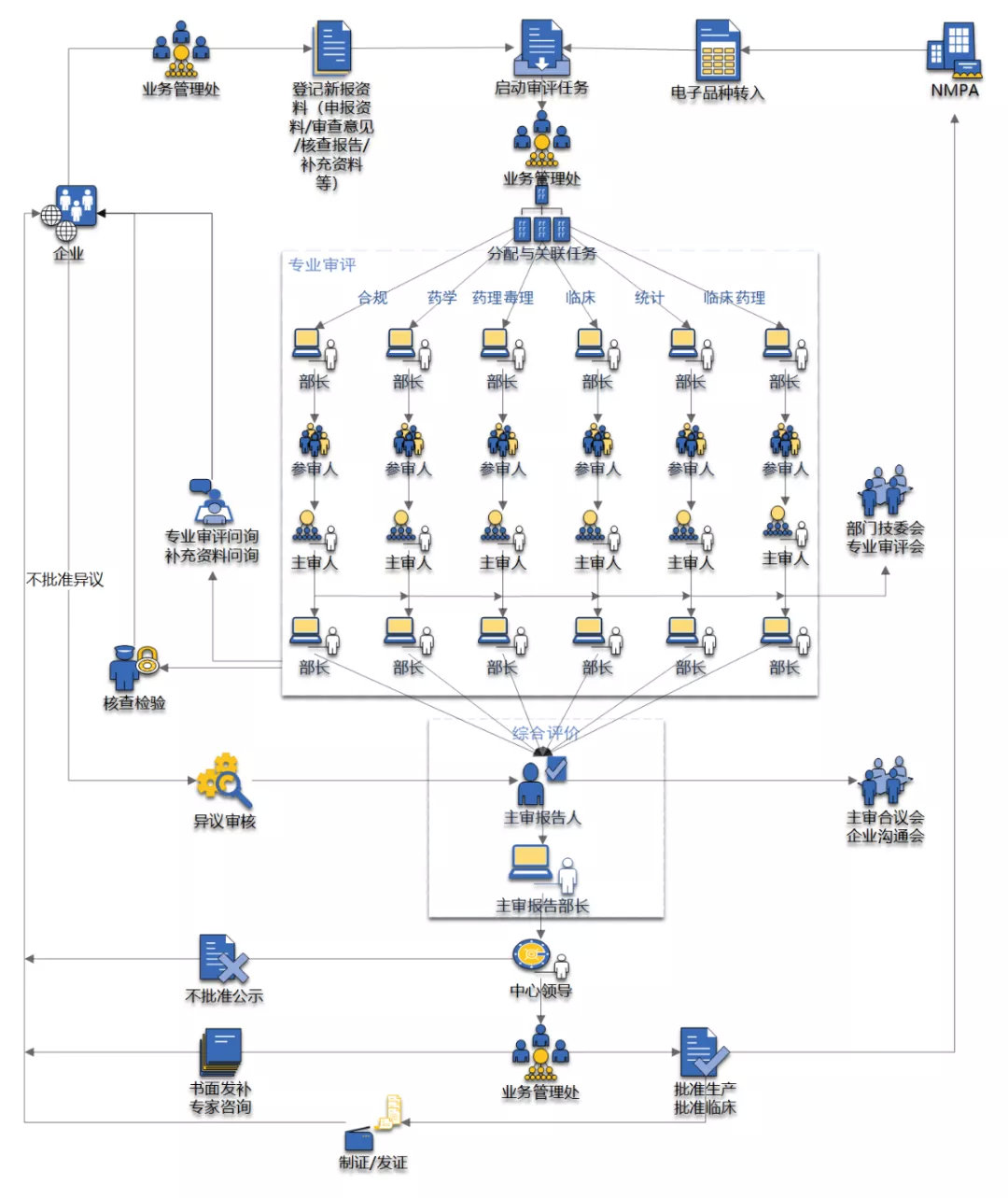
审评工作程序
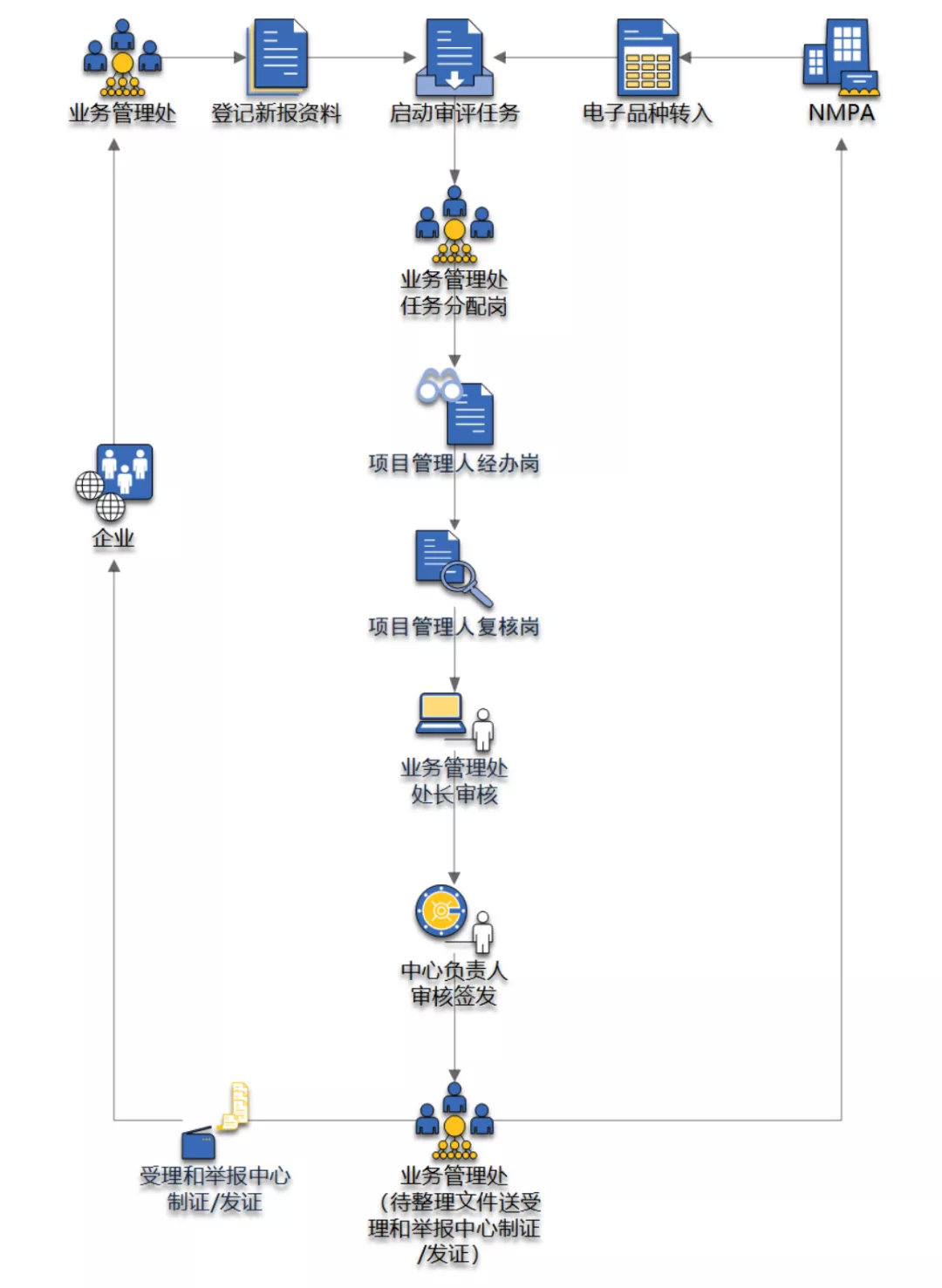
行政审批备案工作程序
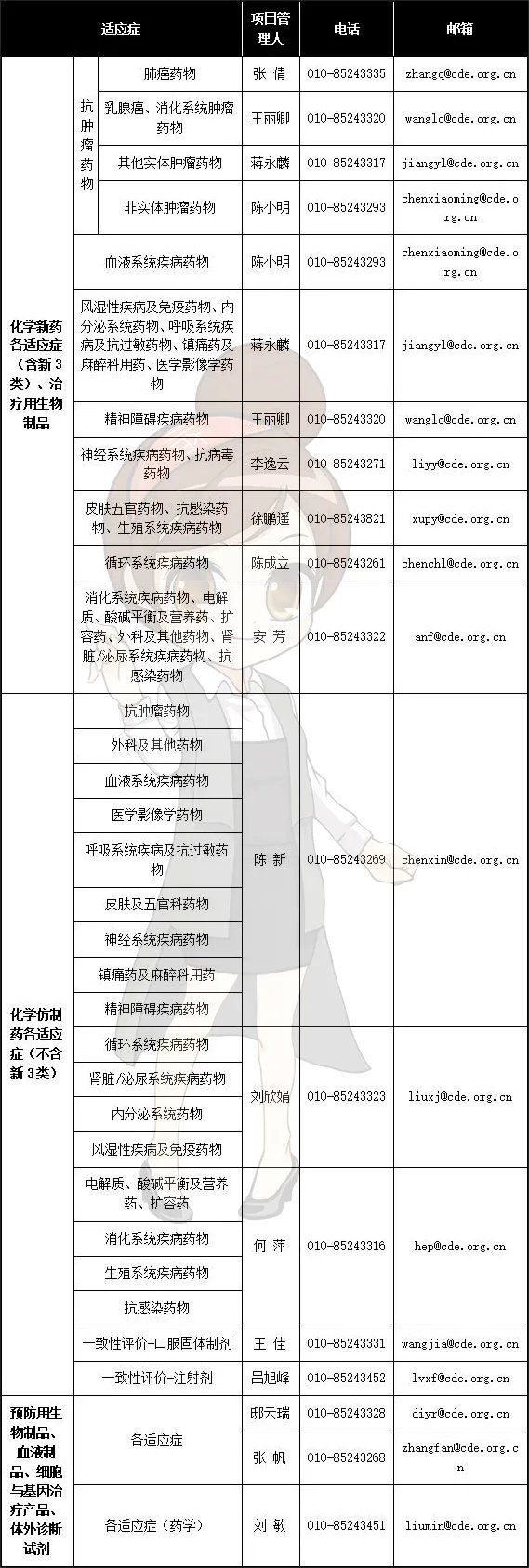

在审化药新药注册申请相关问题:huayaoxinyao@cde.org.cn
在审化药仿制药注册申请相关问题:huayaofangzhiyao@cde.org.cn
在审生物制品注册申请相关问题:shengwuzhipin@cde.org.cn
在审中药注册申请相关问题:zhongyao@cde.org.cn
在审一致性评价注册申请相关问题:yizhixingpingjia@cde.org.cn
原辅包登记相关问题:yuanfubao@cde.org.cn
注册法规相关问题:zhucefagui@cde.org.cn
新冠肺炎药物相关问题:xinguanfeiyanyaowu@cde.org.cn
来源:药物临床试验网


站点声明
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
思途医疗科技有限公司专注于医疗器械产品政策与法规规事务服务,提供产品注册备案申报代理、临床试验、体系建立辅导、分类界定、申请创新办理服务。

以下对欧代、英代简单介绍,下期将针对欧洲注册、英国注册的要求推出详细的专题讲解,包括符合性声明、标签、文件等。"
思途给大家提供免于医疗器械注册质量管理体系核查相关说明的全文内容和文档下载,如果您有免于医疗器械注册质量管理体系核查相关说明的相关临床需求请及时找思途,关注思途了

为落实《医疗器械监督管理条例》(国务院令第739号)要求,根据《医疗器械注册与备案管理办法》(市场监管总局令第47号)《体外诊断试剂注册与备案管理办法》(市场监管总局令第48号),

为落实《医疗器械监督管理条例》(国务院令第739号)要求,根据《医疗器械注册与备案管理办法》(市场监管总局令第47号)和《体外诊断试剂注册与备案管理办法》(市场监管总局令第48号
为贯彻落实《河南省人民政府推进政府职能转变和“放管服”改革协调小组办公室〈关于做好相关问题整改进一步完提升网上政务服务能力的通知〉(豫“放管服”组办〔2019〕7号)》文件

为有效预防、及时控制和消除突发公共卫生事件的危害,确保突发公共卫生事件应急所需医疗器械尽快完成审批并上市使用,根据《医疗器械监督管理条例》《医疗器械注册管理办法》

项目管理是一个在外行看来,非常高大上,随随便便月入几万。在刚入行的人看来,又苦又累还各种求人,就像是在打杂。其实这些都很片面,项目管理入门简单,做好却很难。做项目

近期广西药监局先后发布新冠肺炎疫情防控用应急审批医疗器械注册证和生产许可证延续条件和补充条件两个通知,将应急审批医疗器械注册证注意事项归纳的明明白白。"

为有效预防、及时控制和消除突发公共卫生事件的危害,确保突发公共卫生事件应急所需医疗器械尽快完成审批,根据《医疗器械监督管理条例》(国务院令第739号)及《医疗器械注册

关于公布2024年下半年人类遗传资源行政许可审批受理截止时间计划的通知为进一步提高人类遗传资源行政许可审批的服务质量,方便申请者了解审批进度,现将2024年下半年人类遗传资源行政许可审批受理截止时间计划公布。以下受理截止时间均为当天16:30,如遇特殊情况需调整时间,将提前进行通知。批次受理截止时间2024年第13批2024年06月27日2024年第14批2024年07月11日2024年第15批2
六年
医疗器械服务经验
联系思途,免费获得专属《落地解决方案》及报价
咨询相关问题或咨询报价,可以直接与我们联系
思途CRO——医疗器械注册临床第三方平台