医疗器械注册证信息怎么查询?
医疗器械注册证是依照法定程序,对拟上市销售、使用的医疗器械的安全性、有效性进行评价,决定同意其销售、使用后发放的证件,由国家食品药品监督管理总局统一制定。"
来源:医疗器械注册代办 发布日期:2025-02-09 阅读量:次
引言:医疗器械的分类判定是产品上市前的核心环节,直接影响注册路径与周期。若企业因分类判断失误将Ⅲ类器械误定为Ⅱ类,可能导致注册资料被驳回,甚至面临监管处罚。2021年某省药监局通报的案例显示,一家企业因将可吸收骨填充材料错误归类为Ⅰ类器械,导致产品上市延迟18个月,直接经济损失超千万元。此类教训揭示:精准分类是医疗器械合规进程的第一道生死线。

1、注册延迟:分类错误需重新提交技术资料,平均延长审批周期6-12个月。
2、处罚风险:依据《医疗器械监督管理条例》,故意降低管理类别的企业最高可处货值金额20倍罚款。某跨国企业曾因未申报激光治疗仪的Ⅲ类属性,被处以320万元行政处罚。
1、风险分级制度
Ⅰ类(低风险):非接触人体器械(如外科纱布)
Ⅱ类(中风险):短期接触体内器械(如血糖仪)
Ⅲ类(高风险):植入器械或生命维持设备(如心脏支架)
2、技术参数阈值
侵入深度:表皮接触(Ⅰ类) vs 血管内介入(Ⅲ类)
使用时长:<30分钟(Ⅱ类) vs >30日(Ⅲ类)
能量风险:无源器械(Ⅰ类) vs 放射治疗设备(Ⅲ类)
《医疗器械分类目录》2023版更新要点:
1、新增人工智能辅助诊断软件条目,明确其根据诊断疾病严重性划分Ⅱ/Ⅲ类
2、调整医美器械界定标准,将注射用透明质酸钠从Ⅲ类降为Ⅱ类
判定工具推荐:
1、国家药监局数据库(每季度更新)
2、第三方分类查询系统(需选择NMPA认证服务商)
自主判定 官方界定
适用情形 目录明确产品 创新型/跨界产品
耗时 即时 30工作日
材料 无 产品原理图+风险分析报告
注:2023年官方分类界定驳回率达41%,主要因企业未提供生物相容性试验数据
案例1:AI医学影像系统
1、争议点:肺结节筛查软件属于Ⅱ类orⅢ类?
2、判定依据:FDA将辅助筛查划为Ⅱ类,但中国根据肺癌致死率归入Ⅲ类
3、解决方案:通过分类界定申请补充临床数据,最终获批Ⅲ类
案例2:抗菌涂层缝合线
1、争议点:按医疗器械or药品监管?
2、判定规则:主要作用方式为物理闭合(器械属性),涂层抗菌为辅助功能
3、结果:归入Ⅲ类器械,需提交药物载体释放动力学数据
1、预咨询机制:在研发阶段向省级技术审评中心提交产品描述,获取非正式分类建议
2、国际对标法:参考FDA产品代码(Product Code)与欧盟MDR分类规则,建立分类逻辑矩阵
3、文件留痕:完整保存分类判定过程记录,包括内部评审会议纪要、外部专家意见
某上市企业建立分类决策树工具,使分类准确率从63%提升至92%
建立三层验证体系:
1、基础层:比照《分类目录》关键词检索
2、技术层:分析产品与目录案例的结构等效性
3、决策层:运用监管机构发布的分类界定复函建立案例库
医疗器械分类存在显著地域差异:同一款血糖监测仪,在中国属Ⅱ类需省级审批,在美国为Ⅰ类仅需备案,在欧盟则根据采血深度可能归入Ⅱa类。这种差异源于各国医疗事故数据的积累方向不同。企业开展全球注册时,须建立分类映射表,例如将中国Ⅲ类器械对应FDA的PMA路径。掌握这些规律可减少30%以上的重复申报工作。

站点声明
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
思途医疗科技有限公司专注于医疗器械产品政策与法规规事务服务,提供产品注册备案申报代理、临床试验、体系建立辅导、分类界定、申请创新办理服务。

医疗器械注册证是依照法定程序,对拟上市销售、使用的医疗器械的安全性、有效性进行评价,决定同意其销售、使用后发放的证件,由国家食品药品监督管理总局统一制定。"
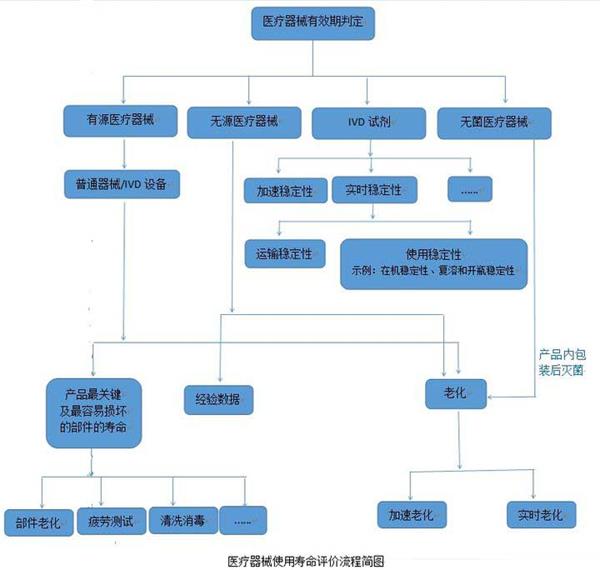
医疗器械的使用寿命是指医疗器械从规划、设计、生产、销售、安装调试到使用、维修、维护检测、报废的全过程。而医院使用的医疗器械的应用质量和安全管理在整个寿命过程中占重

随着医疗器械出口的日益增长,根据市场的需求各医疗器械生产厂商需要符合国家和地区的质量体系法规越来越多,所以经常会碰到出处于不同法规或标准的一些比较容易混淆的概念及

从事医疗器械注册的小伙伴们可能都为同一个问题苦恼过,那就是医疗器械注册单元的划分。企业所设计开发出的产品,其所包含的产品范围,是否可通过一个注册单元完成注册,从而

刚接触医疗器械CRO行业的小伙伴,在学习文件法规资料的同时,常看到一些英文类专业名词不知道是什么意思。下面,一起看看常见的医疗器械临床试验专业术语......"

医疗器械注册检验报告的有效期,行业内常听到各种说法,一起来看一下效期是怎么规定的。"

在之前的文章中为大家简单介绍了国内医疗器械注册证的查询方法,很多读者表示非常实用,受益匪浅,但对于从事医疗器械研发工作的朋友们来说,他们希望获得更多的医疗器械信息

2019年5月31日,国家药监局发布了《关于实施医疗器械注册电子申报的公告(2019年第46号)》,从2019年6月24日正式实施电子申报,从11月1日起提交国家局的注册资料都需要按照电子申报目录

任何国家医疗器械产品出口澳大利亚,需经历TGA注册,以下是关于澳大利亚医疗器械注册知识点,简单了解一下,文中大致概括了注册全流程,未标明细节,如有产品需要澳大利亚注册

早在2017年11月24日CFDA和卫计委就联合发布《医疗器械临床试验机构条件和备案管理办法》(2017年第145号),把临床试验机构的资格认定,改为备案管理。目前,医疗器械临床试验机构备案
六年
医疗器械服务经验
联系思途,免费获得专属《落地解决方案》及报价
咨询相关问题或咨询报价,可以直接与我们联系
思途CRO——医疗器械注册临床第三方平台