医疗器械注册证信息怎么查询?
医疗器械注册证是依照法定程序,对拟上市销售、使用的医疗器械的安全性、有效性进行评价,决定同意其销售、使用后发放的证件,由国家食品药品监督管理总局统一制定。"
来源:医疗器械注册代办 发布日期:2025-01-02 阅读量:次
医疗器械的安全性与有效性直接关系到公众健康和生命安全,因此其生产过程必须遵循严格的标准。在众多保障措施中,医疗器械GMP(Good Manufacturing Practice,良好的作业规范)扮演着至关重要的角色。如果说医疗器械唯一标识(UDI)是医疗器械的身份证,那么GMP就是医疗器械生产企业的通行证,它是医疗器械生产和质量管理的基础,也是医疗器械生产企业准入和日常监督检验的法定依据。本文将深入探讨医疗器械GMP的起源和发展历程,揭示这一关键制度如何在全球范围内逐步建立并完善,最终成为现代医疗器械行业不可或缺的一部分。

GMP的概念最早可以追溯到20世纪中叶,当时随着制药行业的快速发展,人们开始意识到药品生产过程中存在诸多风险因素,如污染、混淆和人为错误等。为了应对这些问题,美国食品药品监督管理局(FDA)率先于1963年颁布了针对药品生产的GMP法规。这一举措标志着GMP作为一种科学的质量管理方法正式登上历史舞台。随后,随着医疗器械技术的进步及其应用领域的不断扩大,各国逐渐认识到有必要将GMP原则应用于医疗器械领域,以确保产品的质量和安全性。
美国作为全球领先的医疗科技强国之一,在医疗器械GMP方面同样走在前列。早在1978年,美国就施行了《医疗器械生产质量管理规范》(GMP),并在1996年对质量管理体系单独立法,公布了《医疗器械质量体系法规》(QSR)作为强制执行的要求。这不仅体现了美国政府对于医疗器械安全性的高度重视,也为其他国家提供了宝贵的经验借鉴。与此同时,日本也在上世纪九十年代确立医疗器械GMP为核发许可证的必要条件,通过立法手段强化了对医疗器械生产的监管力度。这些国家的先行探索为后来者铺平了道路,促进了全球医疗器械GMP标准的统一化和规范化进程。
相比之下,中国的医疗器械GMP起步较晚。直到2009年12月16日,国家食品药品监督管理局印发了《医疗器械生产质量管理规范(试行)》以及《医疗器械生产质量管理规范检查管理办法(试行)》,并于2011年1月1日起正式施行。该文件明确规定,自2011年7月1日后,未达到规范要求的企业将不允许注册。这一政策的出台标志着中国医疗器械强制进行GMP认证时代的来临,开启了国内医疗器械行业从粗放型向精细化管理转变的新篇章。此后,中国不断加强对医疗器械GMP的研究和实践,逐步建立起一套符合国情且与国际接轨的质量管理体系,推动了整个行业的健康发展。
医疗器械GMP涵盖了一系列广泛的管理要求,包括但不限于机构与人员、厂房与设施、设备、文件管理、设计开发、采购、生产管理、质量控制、销售和售后服务、不合格品控制、不良事件监测、分析和改进等方面。这些规定旨在确保医疗器械在整个生命周期内的安全性和有效性,并特别针对无菌产品、植入产品、体外诊断试剂产品、义齿产品、计算机软件等12个方面提出了特殊的要求。通过对各个环节实施严格的控制措施,GMP能够有效降低生产过程中的各种风险,防范污染、混淆、人为差错等问题的发生,从而提升产品质量和服务水平。
随着全球化进程的加速,医疗器械国际贸易日益频繁,各国之间的合作交流也愈加紧密。在此背景下,医疗器械GMP逐渐成为一种国际通用的语言,被越来越多的国家和地区所采纳。它不仅是企业进入国际市场的重要通行证,也是各国监管部门之间相互认可的基础。通过推行统一的质量管理标准,不仅可以促进贸易便利化,还可以加强跨国界的监管协作,共同维护全球公共卫生安全。GMP还有助于推动技术创新和技术转移,鼓励企业不断提升自身的研发能力和生产工艺水平,为行业发展注入新的动力。
医疗器械GMP起源于对药品生产质量管理的需求,并随着医疗器械技术的发展而逐步扩展至该领域。从美国和日本等发达国家的早期探索,到中国近年来的快速追赶,GMP已经成为全球医疗器械行业不可或缺的一部分。通过设立明确的管理要求和特殊规定,GMP不仅保障了产品的安全性和有效性,还促进了行业的规范化、科学化和制度化发展。同时,GMP的国际化趋势也为医疗器械企业提供了更广阔的市场空间和发展机遇,推动了整个行业的持续进步。

站点声明
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
思途医疗科技有限公司专注于医疗器械产品政策与法规规事务服务,提供产品注册备案申报代理、临床试验、体系建立辅导、分类界定、申请创新办理服务。

医疗器械注册证是依照法定程序,对拟上市销售、使用的医疗器械的安全性、有效性进行评价,决定同意其销售、使用后发放的证件,由国家食品药品监督管理总局统一制定。"
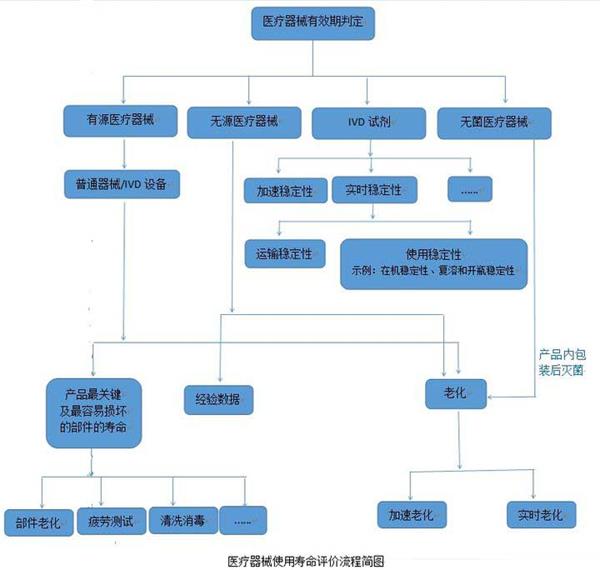
医疗器械的使用寿命是指医疗器械从规划、设计、生产、销售、安装调试到使用、维修、维护检测、报废的全过程。而医院使用的医疗器械的应用质量和安全管理在整个寿命过程中占重

随着医疗器械出口的日益增长,根据市场的需求各医疗器械生产厂商需要符合国家和地区的质量体系法规越来越多,所以经常会碰到出处于不同法规或标准的一些比较容易混淆的概念及

从事医疗器械注册的小伙伴们可能都为同一个问题苦恼过,那就是医疗器械注册单元的划分。企业所设计开发出的产品,其所包含的产品范围,是否可通过一个注册单元完成注册,从而

刚接触医疗器械CRO行业的小伙伴,在学习文件法规资料的同时,常看到一些英文类专业名词不知道是什么意思。下面,一起看看常见的医疗器械临床试验专业术语......"

GMP、GLP和GCP是什么?GMP(GOOD MANUFACTURING PRACTICE)良好生产规范:世界卫生组织将GMP定义为指导食物、药品、医疗产品生产和质量管理的法规。GMP要求制药、食品等生产企业应具备良好的

医疗器械注册检验报告的有效期,行业内常听到各种说法,一起来看一下效期是怎么规定的。"

不少朋友问我,什么是SSU,SSU的CRA能去吗,SSU的PM能去吗?在这里,小君就切身经历对SSU的接触,介绍给大家,如果有说得不对或认识错位,欢迎在评论区撕逼!"

在之前的文章中为大家简单介绍了国内医疗器械注册证的查询方法,很多读者表示非常实用,受益匪浅,但对于从事医疗器械研发工作的朋友们来说,他们希望获得更多的医疗器械信息

2019年5月31日,国家药监局发布了《关于实施医疗器械注册电子申报的公告(2019年第46号)》,从2019年6月24日正式实施电子申报,从11月1日起提交国家局的注册资料都需要按照电子申报目录
六年
医疗器械服务经验
联系思途,免费获得专属《落地解决方案》及报价
咨询相关问题或咨询报价,可以直接与我们联系
思途CRO——医疗器械注册临床第三方平台