有源医疗器械加速老化试验效期验证及使用期限验证流程
为了确保医疗器械在生命周期内的安全及有效性,注册人应在设计开发中对其使用期限予以验证。使用期限的验证是医疗器械可靠性研究的重要组成部分,制定并验证合理的使用期限有
来源:医疗器械注册代办 发布日期:2023-10-10 阅读量:次
去年年底的一颗炸雷,威力震慑了整个医疗器械圈。这颗雷是什么?莫过于2020年12月21日国务院通过的《医疗器械监督管理条例》2020修订版,那时圈内有消息称年后必出正式稿,结果等了个寂寞。当这个消息已经无人关注的时候,某微信公众号在小伙伴等待了将近4个月之久后,又一颗平地惊雷,文件一出,本人东看看国务院官网,西找找药监局官网,愣是没找到正式稿出处。在看完正式稿后,我懵了,修改稿中的二类上报国家局在这份文件中依旧是省局申报,持着将信将疑的态度,我盯了省局老师朋友圈一上午,对,一上午,在省局药监老师转发到朋友圈后,大彻大悟,没错就是它。

本篇文章我们重点关注临床试验机构备案方面内容,第二十六条提到:
开展医疗器械临床试验,应当按照医疗器械临床试验质量管理规范的要求,在具备相应条件的临床试验机构进行,并向临床试验申办者所在地省、自治区、直辖市人民政府药品监督管理部门备案。接受临床试验备案的药品监督管理部门应当将备案情况通报临床试验机构所在地同级药品监督管理部门和卫生主管部门。
医疗器械临床试验机构实行备案管理。医疗器械临床试验机构应当具备的条件以及备案管理办法和临床试验质量管理规范,由国务院药品监督管理部门会同国务院卫生主管部门制定并公布。
国家支持医疗机构开展临床试验,将临床试验条件和能力评价纳入医疗机构等级评审,鼓励医疗机构开展创新医疗器械临床试验。

重点我给标红了,(1)医疗器械临床试验机构实行备案管理;(2)国家支持医疗机构开展临床试验,将临床试验条件和能力评价纳入医疗机构等级评审,鼓励医疗机构开展创新医疗器械临床试验。不是所有医疗器械都需要临床试验,反过来想需要临床试验的医疗器械注册上都会有点难度,毕竟临床试验项目生产企业并不擅长,CRO公司就此孕育而生。扯远了,拉回来,说一下医疗器械临床试验机构备案的事,先看目前国内已备案的医疗器械临床试验机构数量,已经达到995家,药物临床试验机构也有1085家了,在我的印象中,年前还相差着几百,一转眼已经进百了。原因我们就不去追究了,但可以看出医疗机构的热情,都想在临床试验领域分取一杯羹。看看隔壁的山东省,鼓励医疗器械办理药物临床试验机构备案,还有奖金,果然啥都是别人家的好。
开展医疗器械临床试验不仅可以支持国家医疗器械事业的发展、振兴民族器械工业、保障人民健康且对医疗机构自身的发展和建设起到积极作用。
1、有利于医院树立品牌权威。提高公众对医院的评价,建立医院在老百姓心中的威信,提升医院的知名度和影响力,进一步实现社会效益和经济效益兼顾。
2、有利于医院开展循证医学研究。循证医学:是指临床医生对患者的诊治都应该有充分的科学依据,任何决策都需建立在科学证据的基础上,而这种科学也是当前最佳证据。近年来,医患关系日趋紧张,采用循证医学的原理和方法来规范医疗服务行为已越来越为人们的共识。
3、有利于提升医院的科研水平。开展临床试验本身就是一项科学研究,开展临床试验为医疗机构提供很好的科研平台,有利于机构多出成果,多出论文。临床试验至少会在两家以上的机构进行试验,有利于加强医疗机构与同行的合作、增加学术交流的机会,取人之长,补己之短,从而提高医疗机构的科研学术水平。
4、有利于医护人员SCI论文的撰写与发表。论文发表是学术成就的一种体现,可以提高自己的知名度,给同行提供学术性的价值参考,并有助于医护人员评职称和晋升。
5、有利于规范医院的伦理工作。随着国家涉及伦理的临床工作及科学研究的审查越来越严格,以及患者医疗知识、法律意识的提高 ,伦理问题越来越突显。通过临床试验机构的备案,更规范医院的伦理工作。
6、有利于促进医护人员合理用械。医务人员参加一项临床时,对该器械的疗效、安全性、用法、疗程及用器械的适应症、禁忌症等有较全面的了解,必然能够更好地运用到患者身上,有利于规避医疗风险。
7、有利于增强医务人员“以患者为中心”的服务理念。临床试验要求受试者入组前必须将实验的详细情况 告知受试者,并签署知情同意书,实验过程中如发生不良事件,研究者应该采取治疗措施并及及时报告,整个过程要为受试者保密,整个过程都要求研究者处处为患者的利益着想。充分尊重患者的权利。增加了以患者为中心的服务理念,缓解了医患关系紧张的局面。
8、有利于医院引进科研人才。临床试验机构需要设立相关配套的独立部门和科室,需要大量相关的专业科研人才,有利于医院以全职和柔性相结合的形式,面向海内外公开招聘高端科研人才。
9、有利于医院提高医疗能力。随着科技水平不断提高,大量创新型产品和治疗手段衍生,有利于医院开展和尝试尚在临床试验阶段的新型治疗方案,从而大大提升医疗能力。
10、有利于医院等级晋升。二级升二甲,二甲升三级,三级升三甲,审评标准有科研管理水平和科研平台加分。
11、增加医院收入水平等等.......
一不小心列出了十条,备案成功院长也感觉倍有面儿,哈哈......像我这种不要脸的还是少数哈。
最近思途也在推进临床机构备案的事,正在合作的已经有几家临床机构了,达成战略合作关系的也不少,CRO公司不缺临床试验单子,缺的是合作的临床机构,这不我们来解决问题了,解决企业自身的问题,也帮忙解决医院难办的问题。最后,插播一条广告,有药物临床试验机构备案和医疗器械临床试验机构备案,你们又搞不定的,找我哦!
临床试验机构备案代办服务

站点声明
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
思途医疗科技有限公司专注于医疗器械产品政策与法规规事务服务,提供产品注册备案申报代理、临床试验、体系建立辅导、分类界定、申请创新办理服务。
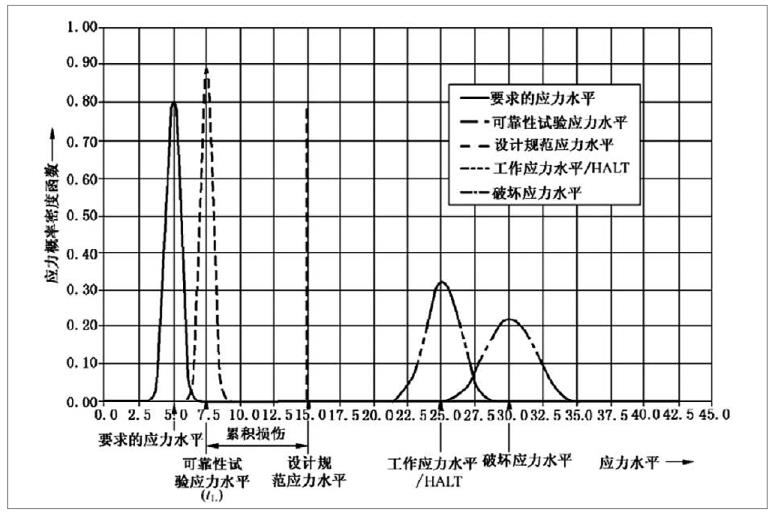
为了确保医疗器械在生命周期内的安全及有效性,注册人应在设计开发中对其使用期限予以验证。使用期限的验证是医疗器械可靠性研究的重要组成部分,制定并验证合理的使用期限有

润滑剂类产品在美国根据产品预期用途的不同主要分为人体润滑剂和患者润滑剂:其中,人体润滑剂主要成分为水、丙二醇、羟乙基纤维素、苯甲酸、卡波姆、氢氧化钠等,作用于生殖

中国能排进世界十大医疗器械制造强国吗?暂时还不能,因为排进前十的国家都有许多知名械企和世界级医疗器械巨头;而中国比较出名的可能只有迈瑞了,其他械企仍需努力了。下面

简述了中药新药临床试验主要特点,指出要重视风险、受益评估,重视人 用经验选择科学、客观、合适的有效性指标,做好中医证候疗效评价,鼓励在中药新药临床研究中采用电子化手

本文介绍了欧盟医疗器械新法规MDR相比于将替代的MDD法规的几点新增要求。建议收藏学习。明年5月份起,Medical Devices Regulation(MDR)(2017/745/ EU)将替代原本的Medical Devices Directive (93
可吸收高分子材料介绍,及其在植入医疗器械中的应用。1、植入产品的定义国家食品药品监督管理局《医疗器械分类规则》(局令第15号)第八条中对“植入器械”的定义为:任何借助

生物材料在疾病治疗和医疗保健中发挥了重要的作用,按材料性质,生物材料可分为惰性材料与可降解性材料两种,目前生物材料的发展呈现出由惰性向可降解性(水解和酶降解)转变的趋

医疗器械注册费是行政性收费,按照注册单元收取,部分省份不收取医疗器械注册费用,绝大部分省份还是收取的。本篇文章统计了截止到2022年1月5日各地医疗器械注册收费标准。

一个产品带有CE 标志(标记) 也就意味着其制造商宣告:该产品符合欧洲的健康、安全、与环境保护之相关法律中所规定 的基本要求。因而该产品是对:使用者(译者注:人)、宠物(

2021年2月5日,湖南省药监局分别与湖南省计量检测研究院、湖南新领航检测技术有限公司、湖南普瑞玛药物研究中心有限公司、深圳华通威国际检验有限公司、南德认证检测(中国)有限公
六年
医疗器械服务经验
联系思途,免费获得专属《落地解决方案》及报价
咨询相关问题或咨询报价,可以直接与我们联系
思途CRO——医疗器械注册临床第三方平台