海南博鳌乐城国际医疗旅游先行区医疗机构制剂调剂使用管理暂行办法(琼药监注〔2020〕16号)
《海南博鳌乐城国际医疗旅游先行区医疗机构制剂调剂使用管理暂行办法》已经3月24日海南博鳌乐城国际医疗旅游先行区领导小组会议审议通过,现印发给你们,请遵照执行。
来源:医疗器械注册代办 发布日期:2020-09-24 阅读量:次
附件:个性化匹配骨植入物及配套工具医工交互质控审查指导原则(2020年第62号).doc
本指导原则是对注册申请人和审查人员的指导性文件,但不包括注册审批所涉及的行政事项,亦不作为法规强制执行,如果有能够满足相关法规要求的其他技术论证方法,也可以采用,但是需要提供详细的研究资料和论证资料。企业应在遵循相关法规和技术标准的前提下使用本指导原则。
本指导原则旨在为注册申请人/生产企业参考《无源植入性骨、关节及口腔硬组织个性化增材制造医疗器械注册技术审查指导原则》(国家药品监督管理局通告2019年第70号)要求进行相关产品的注册申报提供技术指导,同时也为药品监督管理部门对注册申报资料的审评提供技术参考。本指导原则系对个性化匹配骨植入物及配套工具设计开发医工交互的通用指导,以确保研发资料内容的质量,并非注册申报资料的内容格式。注册申请人应依据具体产品的特性对研发资料内容进行充实和细化,并依据具体产品的特性确定其中所适用的细节内容。若不适用,需具体阐述理由并提供相应的科学依据。本指导原则主要针对患者匹配产品,定制式产品也可借鉴本导则。从事生产个性化匹配骨科植入物及配套工具的企业应当遵循《医疗器械生产质量管理规范》(国家食品药品监督管理总局通告2014年第64号)及其相关附录,并具有生产非定制式产品的资格。
本指导原则是在现行法规和标准体系以及当前科学认知水平下制定的,是对个性化匹配骨植入物及配套工具医工交互质量控制原理的进一步阐释,所例举产品有限,尚不能涵盖所有个性化匹配骨植入物及配套工具产品细节,对于某些专项问题的处理方法,尚需针对性的指导原则进行深入论述。随着法规和标准的不断完善,以及技术审评科学的不断发展,本指导原则相关内容也将进行适时的调整、补充和更新。
本指导原则适用于个体化下颌骨假体、定制正颌导板及钛板、髋臼周围型肿瘤髋关节假体、骶骨肿瘤假体、个性化匹配多节段人工椎体等个性化匹配产品及配套工具的设计开发,符合YY/T 0287-2017《医疗器械 质量管理体系 用于法规的要求》中相关基本原则和阶段划分,针对个性化匹配产品进行了具体细化及调整。本指导原则聚焦于“医工交互”的内容,故暂不包括对生产“转换”阶段的讨论,不限于增材制造(3D打印)等具体的生产加工工艺。
本指导原则正文将按照骨植入物和工具分别加以说明,阐述各阶段的医工职责及交互内容,附件中列出了典型产品的医工交互流程图,以供参考。
(一)个性化匹配骨植入物设计程序
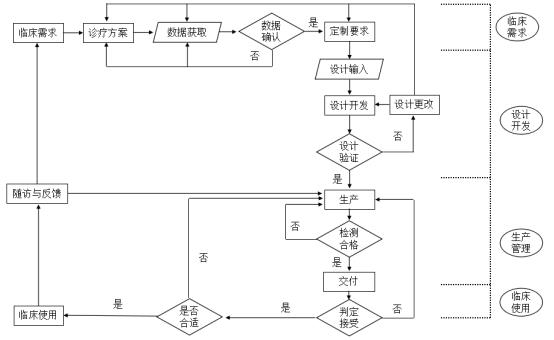
个性化匹配骨植入物的通用设计程序如图1所示,包括策划、输入、输出、验证和确认五个主要步骤;在验证不满足要求的情况下,触发修改工作;根据前序已植入产品临床随访结果,对后续的实施病例的产品进行设计更改;设计程序的所有步骤都在评审监督下开展;所有流程都需进行记录与留样。其中,骨植入物的“输出”结果将触发配套工具的设计程序。
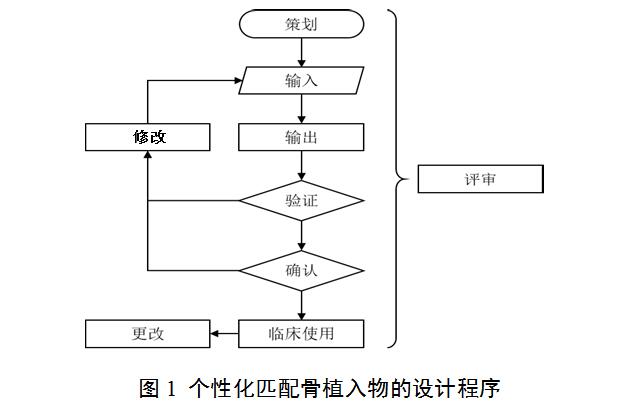
策划步骤主要包括参与人员资质核验、策划立项论证、手术方案规划设计验证要求、产品确认要求等;输入步骤主要包括影像学输入、患骨三维重建、骨植入物设计与分析(包括硬/软组织的固定位置/附着点数量)等;输出步骤主要包括产品三维CAD模型、产品使用说明和终产品检验要求等;验证步骤主要包括背对背盲态设计交叉复验和伴随样品的理化性能测试;确认步骤主要包括终产品与设计结果的吻合性和灭菌确认等;修改步骤需明确其触发条件和修改工作内容等;更改步骤主要包括临床随访记录、更改建议等;评审步骤需明确评审内容和评审方式;记录与留样步骤需明确记录形式和留样规定。
各步骤的程序文件应明确该工作的触发条件、必经步骤及结束条件,以及与相邻方面的衔接过渡,并建立流程图(见本导则各附件)。
(二)个性化匹配骨植入物配套工具设计程序
个性化匹配骨植入物配套工具设计程序如图2所示,其设计程序由骨植入物的输出结果启动,包括策划、输入、输出、验证和确认五个主要步骤;在验证不满足要求的情况下,触发修改工作;根据前序已完成手术患者的临床随访结果,对后续的实施病例的产品进行设计更改;设计程序的所有步骤都在评审监督下开展;所有流程都需进行记录与留样。各步骤工作内容与骨植入物设计程序类似,各步骤的程序文件应明确该工作的触发条件、必经步骤及结束条件,以及与相邻方面的衔接过渡,并建立流程图(见本导则各附件)。
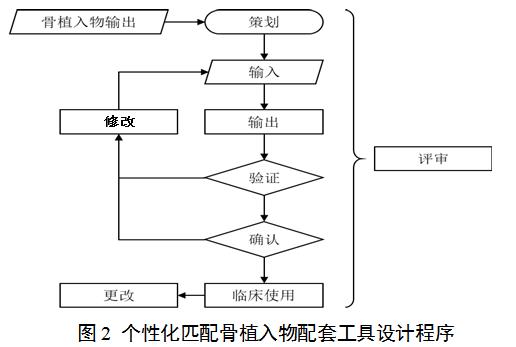
对主持和参与个性化匹配骨植入物及其配套工具设计制作的医工双方人员的资质要求:“医”方建议由三甲医院中具有正高级职称的医生主持个性化匹配骨植入物及其配套工具的全部流程,该医生团队应有运用传统标准化产品开展同等病患部位与病情下类似手术的既往经验;“工”方参与人员需具有个性化匹配骨植入物设计经验或具有3年以上类似植入术式的非个性化匹配植入物的设计与开发经历。
策划文件应对“医”和“工”的工作内容传接过渡做出明示,应有针对性的培训及周期性考核计划,可考虑运用虚构的测试模块,对医工的输入、输出及评审等能力进行模拟测评。
策划文件的文本内容应事先确立标准化格式,至少包括依解剖部位细分的产品设计立项文件和确认文件,立项文件至少包括个性化骨植入物治疗的必要性论证、个性化骨植入物治疗的可行性论证,并按照YY/T0316设定风险分析和管理计划。针对每一名病患的每一件产品即为一项个性化匹配项目,故格式化文本应覆盖所有可能的解剖细分区域。
(一)个性化匹配骨植入物的策划
个性化匹配骨植入物的立项论证内容需包括个性化骨植入物治疗的必要性论证,所拟采用治疗方案是否有已注册的非个性化产品可用,是否通过个性化骨植入物可以显著提高医疗效果,应当通过对比现有非个性化匹配产品与个性化匹配产品的优点和局限性来论证个性化匹配设计的必要性。相较于常规产品,个性化产品带有风险不确定性,应注意避免滥用。
个性化匹配骨植入物的立项论证需包括个性化骨植入物治疗的可行性论证,所拟采用的治疗方案和个性化骨植入物在材料性能、力学性能、特征结构的可制造性,明确医生可接受功能与工程师可以实现能力和可用资源是否匹配;工程上能否在限定时间内提供质量合格的个性化产品;个性化产品在价格上患者是否可以承受,等等。
1.医方职责
(1)个性化匹配植入产品的策划过程中,医生以及医生所在单位主体应该具有具体个性化定制的能力与经验,多数骨科植入物为永久植入式,因此在策划个性化匹配产品时,主刀医生要对类似治疗经验进行临床评价,提出理论依据,证实拟实施的个性化治疗方案的的必要性和可行性。
(2)策划立项文件中需提出治疗目标,论述患者的整体情况,目标区域的解剖及生理功能特点,相邻区域的解剖、生物力学参数,并对可能考虑到的健侧/对侧的因素进行充分陈述。在植入物设计过程中应注意,医生考虑的综合问题与工程人员关注的局部设计常常存在偏差。
(3)策划立项文件中应提出植入物设计需要考虑的要求,包含质量、性能、材料、尺寸、安装定位方式等。
(4)策划立项文件中需明确手术方案规划,特别注意个性化骨植入物与软组织、硬组织的固定方案。
2.工程师职责
(1)根据医生需求,为其提供骨植入物材料、植入物设计、工程分析、制造可行性等方面的支撑,论证个性化骨植入物治疗实施的工程可行性;协助医生确定是否能够在限定时间内完成制造并进入临床应用;估算成本价格。
(2)与医生明确个性化匹配骨植入物设计的适用范围,告知现有已注册的生物医用材料和制造工艺在力学性能、表面粗糙度、制造精度上是否满足要求;明确骨植入物设计制造中可能的技术风险及控制措施并告知医生。
(3)按照程序流程形成设计开发计划,主要包括设计实现技术路线和项目时间节点。设计实现技术路线应定义每个设计阶段的验证、确认与设计转换所必需的活动类别,包括有限元分析、疲劳测试、模拟手术及构件试样/原型产品的生产等方面的参数赋值。
3.医工交互内容
(1)共同论证个性化植入物设计制作的可行性。根据现有技术储备(包括原材料、终产品性能、工艺水平、使用软件、设计能力),确定个性化植入物实施的可行性。
(2)手术方案交互。对于个性化植入物手术方案的规划,医工交互过程中医生应详细充分地告知工程人员手术规划的诸多细节问题,防止因常识性理解误差或专业性角度差别造成认知差异,防止因工程人员未考虑到某些未告知的因素,所设计植入物在操作过程中出现不合理现象。手术规划应明确限定病患影像数据获取到植入物及工具设计确认、设计确认到手术日之间的时限,具体到自然日,以减少病情变化对设计有效性的影响。
(3)共同确立设计实现技术路线。定义每个设计阶段的验证、确认与设计转换所必需的活动类别,包括有限元分析、疲劳测试、模拟手术及构件试样/原型产品的生产等。
(二)个性化匹配骨植入物配套工具的策划
个性化匹配骨植入物配套工具需起草单独的立项策划文件,其必要性应结合个性化匹配骨植入物的策划文件进行论述。
1.医方职责
(1)医生应在策划文件中明确个性化配套工具使用的必要性。
(2)个性化配套工具的设计过程中,医生应该在与工程人员充分沟通手术方案及细节后,告知工程人员配套工作的具体功能作用,以及辅助工具具体参与的操作环节,可能涉及的操作区域以及操作人员(有时需要护理人员设置、组装等等)。同时,在设计过程中医生要告知工程人员,除了与植入物的匹配,还要考虑使用过程中操作者把持的安全、简捷、方便、舒适以及可重复性等。
(3)个性化配套工具的策划过程中,医生以及医生所在单位主体应该需要具有个性化定制的能力与经验,因此在策划个性化配套工具时,主刀医生要提出理论依据,并得到工程人员证实该配套工具在设计及制造过程中的可行性。
2.工程师职责
参照个性化匹配骨植入物的策划中的工程师职责。
3.医工交互内容
参照个性化匹配骨植入物的策划中的医工交互内容,应注意个性化匹配骨植入物特殊的手术入路,及其对配套工具设计功能及性能的影响。
(一)个性化匹配骨植入物的输入
个性化匹配骨植入物的输入包括病患处影像学数据、植入物三维模型设计与植入后使用效果分析。
1.医方职责
(1)提供满足病患处三维重建需求、满足植入物三维模型设计精度要求的医学影像数据,提供影像采集过程的主要技术参数,包括患者体位、扫描层厚、扫描间距等。
(2)根据诊疗要求,形成骨植入物的设计需求文件,提出骨植入物设计的依据和设计准则,提出骨植入物拟采用的材料的要求及表面粗糙度要求,指出骨植入物在人体内的受力情况,每一名个体病患的预期运动功能、植入时限、恢复到正常生活的程度(预期的生活质量评分)。
2.工程师职责
(1)形成设计输入文件,应至少包含对设计输出的技术参数及规范的要求,设计所需影像数据的要求,设计原始数据处理的要求和设计开发所需使用的软件和功能模块的要求等。其中,对影像数据的要求应考虑对伪影和噪声的消除,以及增材制造中阶梯效应的减少。软件和功能模块的要求应至少明确所使用的软件和功能模块的名称,版本和定期核查校验的机制。
(2)根据医生所提供的影像学数据对病患部位进行三维重建。需明确原始图像数据的去噪、图像分割算法,三维及多平面重建算法,三维模型的平滑及简化方式等。
(3)根据骨植入物的设计需求文件和病患处三维模型,设计个性化匹配骨植入物的三维模型。
(4)根据病患处三维模型、骨植入物三维模型和骨植入物在人体的受力情况,结合植入物固定方案,开展有限元分析,初步评估植入物在人体内的安全性和有效性,有限元分析的开展及要求参考相关指导原则,本导则第“十一”部分提示了个性化匹配设计运用有限元分析时的一些注意事项,以供参考。
3.医工交互内容
(1)影像输入和三维重建。个性化匹配设计很大程度上依赖影像学数据的产生、处理,及解剖模型和结构组件模型的三维重建。医工双方在影像学数据输入和处理中应确定原始设计数据来源、确定需重建组织的范围、重建模型与原始数据之间的误差允许范围等,对影像采集设备应讨论管电流、管电压、窗宽、窗位等参数是否能符合数据质量要求,应规范灰度、对比度等参数的调整规则,应预先设定图像处理软件的图像层距、像素值、灰度阈值、三维叠加运算方法,规定主应力区(包括骨断端内固定与近关节面区域)的曲面构造设计、修正的步骤与原则,尤其对镜像修复与点云数据的补充,尽量减少手动分割。
(2)设计准则和依据。医工双方在个性化匹配骨植入物的设计与分析中需明确个性化治疗的要求,确定替代组织结构的设计依据,明确病变组织与替代物的关系(包括硬组织固定方案、软组织固定方案等),指出骨植入物拟采用的材料及其力学性能,明确骨植入物在人体内的受力情况并适当对其进行简化,明确骨植入物的设计分析目标和(或)安全系数,明确对骨植入物设计的安全性和有效性的评价指标。软组织固位孔与螺钉孔在很大程度上影响着假体的负荷环境。软组织固位孔应以恢复假体周围肌肉、韧带等合理解剖位置及力学功能、确保残留软组织覆盖并消除体内死腔为目标。螺钉固定孔设计应考虑固定钉周围骨量最大化,及骨所受应变的限度。工程设计需辅助明确孔分布位置、数量、孔径、孔间距、边距,及匹配内固定钉的几何参数与空间分布。应特别注意由于肌腱、韧带解剖位置改变对假体主应力区带来的特殊的剪切、扭转负荷,还应注意植入物-软/硬组织界面对组织的应力屏蔽风险。
(3)在预期用途、功能性能相对类似的个性化匹配产品集群内,会产生序贯累积的设计信息,所以在输入信息的格式化文本中,应体现前序产品的关键设计信息,尤其是实体主应力区、多孔骨结合区等共性设计区域。
(二)个性化匹配骨植入物配套工具的输入
个性化匹配骨植入物配套工具的输入包括病患处三维模型、骨植入物三维重建模型和手术规划方案。
1.医方职责
(1)医生要详细介绍患者基本特点,告知手术的详细操作流程,通过文件明确配套工具的使用原理、使用方式和拟采用的材料。
(2)医生要明确手术时限、手术条件、手术中拟切除及矫治的范围。
2.工程师职责
(1)根据已设计输出的骨植入物三维模型、病患处三维模型和配套工具的使用方法,设计个性化匹配骨植入物配套工具的三维模型。
(2)涉及手术规划的软件及功能模块应获得产品注册证。
3.医工交互内容
(1)设计准则和依据:医工双方在个性化匹配骨植入物配套工具的设计中需首先明确对应的个性化匹配手术规划流程,手术过程中截骨、骨填充、植入物植入等关键环节,并将其转换为配套工具的解剖定位、测量标记和截骨区域测控组件的设计准则。
(2)临床截骨矫形等手术规划与植入物的骨结合区、解剖匹配区与主应力区,及相应软组织固位孔及螺钉固定孔的设计,有极大关联。截骨、骨填充、植入物置入的需求,应转化为对配套工具的病患解剖定位、测量标记和截骨区域测控组件的设计输入。配套工具并不仅指术中使用工具,还包括模拟手术过程、验证术中工具可用性和植入物适配性的病患解剖结构实物模型。
(3)病患术前术后的运动态与运动功能评估,是个性化匹配手术规划的重要内容,医学方面与工程方面应合作完成评估表,并明确评估内容与植入物和工具设计参数、围手术期康复护理的关联。
个性化匹配设计的骨植入物和配套工具的输出包括设计所使用的医学影像数据、重建的病患部位三维模型、终产品的三维CAD模型(应使用通用三维模型格式,例如IGES、STEP、STL等)和产品使用说明。
个性化匹配设计的输出还包括每件产品的使用说明,说明中需明确产品的设计原则、设计步骤、输入环节中的设计要点、设计分析报告、产品接受准则和检验规则、产品使用方式等。
(一)个性化匹配骨植入物的输出
个性化匹配骨植入物的输出包含重建的病患部位三维模型、终产品的三维CAD模型(应使用通用三维模型格式,例如IGES、STEP、STL等)、产品使用说明。
1.医方职责
医生应在工程人员的帮助下反复观察评估CAD文件,并告知工程人员重要的核心细节的检验要求。医生应明确产品后期的使用。
2.工程师职责
(1)按照程序流程形成设计输出文件,至少应包含设计模型文件,工程图纸,质量核心参数清单,加工工艺流程,生产检验规范和产品使用说明等。
(2)设计模型文件,工程图纸应至少包含设计版本,审核人签字确认和设计日期等信息,确保设计过程可追溯性。
(3)质量核心参数清单应明确所有与终产品质量和使用相关的参数,并明确参数的接受标准。
(4)加工工艺流程应该至少包含加工工艺细节,明确多孔结构的清洗验证、残余应力的后处理、表面改性等特殊工序,明确各加工工序之间的衔接。
(5)每件个性化匹配产品均应有独特使用说明,明确使用边界,包括截骨位置与个性化匹配产品结构的几何尺寸。螺钉等残存骨组织中内固定物的空间位置应有形象的描述图(坐标系及坐标值),明确骨结合区骨小梁多孔结构的孔径、孔隙率、通孔率,明确软组织非附着区的表面粗糙度。
3.医工交互内容
(1)双方共同进行植入物CAD文件的检查。
(2)核心质控参数:确定与终产品质量相关的质控参数,明确参数的接受标准。一定解剖区域的产品应形成统一的设计规范,应明确该类个体化匹配产品的设计原则、设计步骤、输入环节中设计要点细节、产品接受准则及相应的检验规则。
(3)产品使用说明:明确使用边界,包括截骨位置与个性化匹配植入物结构的几何尺寸。螺钉等残存骨组织中内固定物的空间位置应有形象的描述图(坐标系及坐标值),明确骨结合区骨小梁多孔结构的孔径、孔隙率、通孔率,明确解剖匹配填充区的网格结构单元的三维点坐标。为适应术中截骨及固定的可能变化,应有一定尺寸梯度范围内的多个规格的备件。
(二)个性化匹配骨植入物配套工具的输出
个性化匹配骨植入物配套工具的输出包括终产品的三维CAD模型和产品使用说明。
1.医方职责
医生应在工程人员的帮助下反复观察评估配套工具的CAD文件,并在数字三维模型上进行操作验证。针对产品配套工具后期的使用要点,医生要做出清晰明确的说明。
2.工程师职责
(1)按照程序流程形成设计输出文件,至少应包含设计模型文件,工程图纸,质量核心参数清单,加工工艺流程,生产检验规范和产品使用说明等。
(2)设计模型文件,工程图纸应至少包含设计版本,审核人签字确认和设计日期等信息,确保设计过程可追溯性。
(3)质量核心参数清单应明确所有与终产品质量和使用相关的参数,并明确参数的接受标准。
(4)加工工艺流程应该至少包含加工工艺细节。
(5)每件个性化匹配工具均应有独特使用说明,明确使用边界,包括截骨位置与配套工具的几何尺寸。
3.医工交互内容
参照个性化匹配骨植入物的输出中的医工交互内容。
个性化匹配产品设计开发的各阶段均需要医生与工程师的系统评审并构建决策树,主要集中在输入输出验证确认阶段。评审记录应该有模板化格式,记录所有阶段的评审过程与结果,包括每一轮评审发现的问题、整改措施、修正结果,对产品设计规范的调整与改进。
(一)个性化匹配骨植入物的评审
个性化匹配骨植入物的评审主要包括:影像学数据的正确性、病患部位三维模型的准确性和细化程度、植入物设计是否达到预期要求、手术规划与配套工具的匹配性等,并确保各项输入输出都可被验证或确认。特别注意对必要时所进行的设计修改的评审。
1.医方职责
评审过程中医生需要关注的核心问题是输入输出全过程中目标患者的准确无误,患者影像数据获取的正确性、临床诊断与影像诊断的一致性;输出三维模型的准确性(病患部位病理模型的细化程度与准确性),以及植入物与临床预期要求的符合程度。
2.工程师职责
评审过程中工程师需要关注的核心问题是输入输出全过程中图像分割重建、模型构建、镜像拟合重建设计的合理性、植入物各功能区的力学划分合理性,等等。工程师必要时应提出设计修改建议,应对设计更改做出可行性判定,确保各项输入均可最终被验证或确认。
3.医工交互内容
按照程序流程,严格对个性化匹配骨植入物的各个设计阶段的设计结果进行审评,应该共同制定评审记录的模板化格式,记录所有以上方面的评审过程与结果,包括每一轮评审发现的问题、整改措施、修正结果,尤其对产品设计规范的调整与改进。
(二)个性化匹配骨植入物配套工具的评审
个性化匹配骨植入物配套工具的评审应主要关注手术规划与配套工具的匹配性、植入物与3D病理模型的匹配性。
1.医方职责
评审工具与植入物的匹配程度以及工具在手术操作中的实际情况,医生在术前要明确验证,尤其是配套工具与植入物的功能匹配至关重要。
2.工程师职责
参照个性化匹配骨植入物的评审中的工程师职责,各类软件的合理运用、算法的建立与调整、力学区域的划分,以及工艺实现的可行性,都需要工程师评审。
3.医工交互内容
参照个性化匹配骨植入物的评审中的医工交互内容。
不同于批量化重复生产的常规标准化产品,个性化匹配骨植入物及配套工具的验证包含了对“个性化加工制造”的验证,故医生必须参与其中,需对每一件个性化匹配骨植入物及其配套工具的设计分别进行。因而,个性化匹配骨植入物的验证包含了“确保其在服役过程中能够安全、有效地替代缺损部位的功能”的目的,对其验证包括设计开发评价、伴随样品的理化性能测试、产品生物力学性能测试等;配套工具的验证需保证其在手术过程中能够准确实现对截骨等关键步骤的辅助定位,其验证主要通过对辅助工具的使用模拟和手术方案验证。
(一)个性化匹配骨植入物的验证
骨植入物的验证包括以背对背盲态设计交叉复验为主的设计开发评价、伴随样品的理化性能测试、产品生物力学性能测试和手术方案验证。
1.医方职责
(1)植入物验证过程中主导个性化设计的医师应当主动、充分、详细介绍个性化产品的目标、特性、功能以及可能存在的不足,以供同行及上级医生更有效地复验。
(2)通过进行临床医师之间的背对背盲态设计交叉复验,以调整和细化设计规范,减少医师因素造成的个体内差异。除主刀医师,还应引入另一名同资质医师进行交叉设计,差异过大时引入第三名医师,直至差异局限于预定范围内。鉴于满足特定资质的临床医师资源有限,定制医师可能来自于不同医疗机构。因此,交叉设计验证时即应充分运用“多中心”概念,即复验者可盲态来源于其它医疗机构,以更好地明确并控制医师因素造成的个体内差异。无论是多中心形成的个体内差异度,还是个体间差异度,都是临床“确认”时基线风险分析的基础。
(3)验证文件应明确差异限度、交叉复验时限,并规定交叉复验的揭盲程序。对复验出的差异度,应归入历史文档并采取技术手段防止修改。应统计交叉复验的结果,并迭代累积相近病患与产品,明确个体间设计差异度,后续的设计开发“确认”与此相关。
(4)使用3D打印病理制件模拟手术方案,确保植入物与患处软硬组织的匹配。临床影像信息的重复采集与对比,也是对设计模型评价的验证过程。医师将对解剖学及产品预期作用进行评估,验证文件应限定评估量表,明确量化指标。
2.工程师职责
(1)伴随样品的理化性能测试:由于个性化匹配植入物独一无二的特点,对终产品进行直接的物理化学测试在实践中的可行性不高,可通过对伴随样件的理化性能测试,与输入步骤中的有限元分析结果做对比,实现对个性化匹配植入物的安全性的验证,相关要求可参考《定制式个性化骨植入物等效性模型注册资料技术指导原则》(国家药品监督管理局通告2020年第48号)。每项测试应明确抽样量的确定方法,以保证验证结果的稳定性。有限元分析也是力学测试验证的重要工具,也可参考第“十一”部分所提示的个性化匹配设计开发运用有限元分析时的一些注意事项。
(2)产品生物力学性能测试:模拟骨植入物在人体的使用环境,建立相应的测试工装,对骨植入物的力学性能进行测试。若骨植入物中存在多孔的骨结合区,需单独对多孔区域的力学性能进行测试,并进行骨及血管长入的动物实验,以支持骨传导与骨整合作用。鉴于病损匹配的时效要求,这些验证测试均需建立在对既往测试数据分析的基础上,而不宜每件均开展新的。验证文件应细化触发新试验的条件。
3.医工交互内容
(1)伴随样品的理化性能测试:双方共同确定产品理化性能测试的触发条件、产品理化性能的测试内容,测试方法和测试接受条件。
(2)明确对产品的力学性能进行新测试或开展动物试验的触发条件,动物建模应结合解剖部位的病理和生理特点,应关注离体骨小梁结构的力学验证,尤其是骨结合区。
(二)个性化匹配骨植入物配套工具的验证
通过对病患解剖结构三维重建模型的实际操作,验证配套工具的可用性。
1.医方职责
一般应使用3D打印病理解剖制件模拟手术方案,确保配套工具的可用性。
2.工程师职责
参照个性化匹配骨植入物的验证中的工程师职责。
3.医工交互内容
参照个性化匹配骨植入物的验证中的医工交互内容。
个体化匹配产品仅用于某一特定病患,应关注临床确认的抽样统计、代表产品选择、临床评价产品与放行产品的区分。其设计确认重度依赖既有类似病例所累积的治疗数据、仿真台架模型及动物模型力学性能测试,而基本上无法在使用前完成大规模临床研究。确认工作应有更灵活、更严谨并动态调整的临床确认方法,将统计学控制贯穿于全生命周期的确认证据,且应基于相近生物力学功能的、同类个体化匹配产品系列的迭代数据。
(一)个性化匹配骨植入物的确认
针对骨植入物的功能适配性和解剖匹配性,由主刀医生完成术前确认。预先设定确认的内容与参数,植入物的确认围绕临床预期用途展开,并延伸至产品上市后,开展主动的、有计划的上市后临床研究。医工双方需按照既定程序,依据前序产品评价指标的累积汇总数据趋势,持续改进后续个性化匹配骨植入物的设计。个性化匹配产品常带有监管部门的上市后要求,故设计开发确认文件中应对其进行标识并设定执行细则。上市注册前的临床确认工作应符合附带条件批准的法规和技术规章,并转化为与所研发个性化匹配产品相关的内容与参数,制定阶段性临床研究方案,设定期中分析节点及可接受的统计学特征。
1.医方职责
确认环节中,主刀医师首先要确认植入外观、形状以及多孔等功能结构与设计内容和参数的吻合情况,同时要再次确认关键部位的可靠性与安全性,对于使用过程中的关键部位要反复确认并在模型上进行再次确认。
2.工程师职责
(1)按照程序流程对设计过程、生产过程和审评过程的内容进行确认。
(2)应对产品设计输出进行设计确认,需格外注意灭菌确认,对非批量化生产,不建议采取参数放行。设计开发体系文件必须对可能出现的各种定制产品的生物负载限度做出预判,并对相应的灭菌过程与结果进行传统放行确认和详细记录,尤其针对网格或多孔结构等表面积较大的部分,明确开展新的灭菌确认的触发条件。
3.医工交互内容
(1)双方共同确认植入物产品与设计模型的吻合情况,确认关键部位设计的可靠性和安全性;
(2)灭菌确认:对植入物产品的灭菌过程和结果进行确认和记录,针对有多孔结构的部分,明确开展新的灭菌确认的触发条件。
(3)生物统计师应与临床医师预先制定长期临床研究计划与统计分析计划(包括数据统计步长/周期),将上市后不良事件监控及被动追溯,升级为主动的、有计划的上市后临床研究。
(二)个性化匹配骨植入物配套工具的确认
由主刀医生完成配套工具的术前确认,预先设定确认的内容与参数,配套工具的确认围绕手术规划展开。医工双方需按照既定程序,依据前序产品评价指标的累积汇总数据趋势(如手术步骤与特殊入路的经验/教训),持续改进后续个性化匹配配套工具的设计。
1.医方职责
确认环节中主刀医师首先要确认工具与植入物的匹配情况及其安全性。同时,要确认操作使用过程中的安全(核心,包括医护与患者)、简捷(手术辅助医护可能对个性化辅助工作不够熟悉,因此设计的手术步骤不能过于复杂)、方便(个性化手术往往有其特殊之处,因此辅助工具要方便操作)、舒适以及可重复等。
2.工程师职责
参照个性化匹配骨植入物的确认中的工程师职责。
3.医工交互内容
参照个性化匹配骨植入物的确认中的医工交互内容。
个性化匹配产品应确定何种情况下需进行设计修改,确定设计修改工作涉及的设计流程,设计修改结果的验证和确认指标。
(一)个性化匹配骨植入物的设计修改
确定在何种情况下需要对骨植入物进行设计修改,并明确设计修改结果的确认复验的控制指标,双方需对设计修改过程中可能发生的可能发生的力学性能的改变以及对功能微结构的影响进行评估。
1.医方职责
如涉及到设计修改环节,医生需要在转化环节结束后对植入再次进行确认复验,同时要征询工程人员在转化过程中可能发生的力学性能的改变以及对功能微结构的影响。
2.工程师职责
(1)应明确因为设计修改而需要重新进行的设计、生产验证/确认工作。
(2)针对需要重新开展的工作,严格按照前述相应的流程和要求展开工作。特别注意要对加工制造过程的可行性进行验证,确保加工制造过程稳定、受控。
(3)应按照质量体系的要求对文件进行归档处理,确保工作的可追溯性。
3.医工交互内容
(1)确定植入物设计修改后终产品的接受指标,包括产品的制造精度、力学性能、表面改性要求、残余粉末清洗、灭菌要求等。
(2)设计修改过程应按照质量体系要求对文件进行归档,确保可追溯性。
(二)个性化匹配骨植入物配套工具的设计修改
确定配套工具设计修改工作的触发条件,明确设计修改结果的确认复验的指标。
1.医方职责
医生对配套工具的设计修改仍是关注设计修改后与植入物的匹配,以及使用过程中的性能。
2.工程师职责
参照个性化匹配骨植入物的设计修改中的工程师职责。
3.医工交互内容
参照个性化匹配骨植入物的设计修改中的医工交互内容。
每一例产品的设计都要经历前述的设计开发评审、验证和确认的流程。若新产品相较于前序产品,主要功能、软硬组织固定方式的设计发生改变,或临床评价指标的累积数据趋势突破了预设可接受限,应重新分析前序已植入或已使用产品的风险,增加对前序病患的随访时点、随访内容、预防性的干预措施、再干预治疗,并将相关经验纳入后续新产品的设计开发。
(一)个性化匹配骨植入物的更改
1.医方职责
在个性化设计植入的应用随访过程中医生应适时与工程人员沟通交流前序植入物的应用随访情况,并将临床随访数据应用于后续开发设计的改进工作中。因个性化设计的临床数据量有限,更需要临床随访数据的反馈来提高植入物的精确度。
2.工程师职责
(1)应根据风险再评估的结果,确定因为变更而需要重新进行的设计、生产验证/确认工作。
(2)针对需要重新开展的工作,严格按照前述相应的流程和要求展开工作。特别注意要对加工制造过程的可行性进行验证,确保加工制造过程稳定、受控。
(3)应按照质量体系的要求对文件进行归档处理,确保工作的可追溯性。
(4)企业应设定风险再评价的程序与具体分析要点,并对再评价结果与采取的应对措施及影响结果进行记录,应将对历史病例的术后再干预列入临床确认方案中。
3.医工交互内容
(1)双方根据随访过程中存在的问题进行沟通,将随访问题及数据用于后续开发设计的改进工作中。
(2)确保对随访中发现的问题及改进工作的可追溯性。
(二)个性化匹配骨植入物配套工具的更改
1.医方职责
个性化匹配骨植入物配套工具的更改需要临床医生及时将术中操作过程中遇到的问题以及配套工具使用体会告知工程人员,不断提高配套工具的设计。
2.工程师职责
参照个性化匹配骨植入物的更改中的工程师职责。
3.医工交互内容
参照个性化匹配骨植入物的更改中的医工交互内容。
按照解剖部位与功能需求(尤其主应力区),将个性化匹配骨植入物划分为不同的产品族,分别进行设计开发文档的记录和存档,文件存储应严格按照设计开发的时间轴进行存储,避免未经授权的单方面改动。所有改动都不得删除或掩盖原存储内容,所有变更过程都应留下可复查轨迹。个体化匹配设计开发的数据量较大,且可能在医工交互过程中,随病情进展而循环往复进行设计修改或后续产品更改,并与临床长期累积风险的评价紧密相关,故而输入输出的数据及记录须确保可追溯性。同时,数据拥有者可能是多方和多时空分布的,数据的不可篡改性与信息安全性显得尤为重要,鼓励运用区块链等先进的分布式数据管理技术。
(一)个性化匹配骨植入物的记录与留样
植入物的设计开发过程中的原始影像数据、三维模型、有限元分析文件、设计开发文档等应严格按照时间轴进行存储,任何变更过程都应经医工双方核实并留下可复查轨迹。骨植入物的制造过程应有相应留样,留样可为相同完整产品或标准测试样块,任何进行台架力学实验的完整产品或标准测试样块都应有同批留样,禁止事后补制。
1.医方职责
留样环节中医生应全流程把控,首先从患者的影像学数据的获取备份以及设计过程中的所有CAD文件及其衍生数据等,包括打印的病理模型和未使用的备选植入物等,均应在医生参与的过程中留样保存,如留样记录中需医生签字。
2.工程师职责
(1)实际植入产品应在生产制造中有相应留样,生物力学及台架力学验证时,无论完整产品还是测试样块或原型,均应有同批留样,且不能事后进行补制。
(2)设计开发确认过程中所有阶段性统计分析结果,都应及时准确地记录于临床确认文档。
(3)应严格按照质量体系的要求对设计形成的文件进行管理,并采用诸如区块链等分布式数据管理技术,确保数据不可篡改性与信息安全性
3.医工交互内容
(1)双方共同对设计过程中确定植入物制造过程中原始影像数据、三维模型、有限元分析文件、设计开发文档等的变更进行核实。
(2)双方共同确定留样形式与留样数目。
(3)所有阶段性统计分析结果,都应及时准确地记录于临床确认文档,并确保医师、工程师、康复师、护师及统计师签字确认。
(二)个性化匹配骨植入物配套工具的记录与留样
配套工具的设计开发过程中使用的植入物和病患组织三维模型、设计开发文档等应严格按照时间轴进行存储,任何变更过程都应经医工双方核实并留下可复查轨迹。
1.医方职责
每次个性化手术结束后配套工具应与未使用植入物等同时留样保存。
2.工程师职责
参照个性化匹配骨植入物的记录与留样中的工程师职责。
3.医工交互内容
参照个性化匹配骨植入物的记录与留样中的医工交互内容。
有限元分析是在设计开发中评估植入物在人体内的安全性和有效性的重要工具,对于个性化匹配骨植入物的有限元分析工作的开展,应参考以下内容:
1.明确有限元分析的对象、目的及分析结果的评价指标。
2.明确开展有限元分析所使用的软件系统。
3.描述有限元模型的建立依据,需明确指出所建立的有限元模型与实际骨植入物设计模型及其预期使用环境在关键要素上的一致性和差异。以上关键要素包括骨骼的几何模型、植入物几何模型以及有限元模型中的载荷、边界条件、材料属性、装配关系与接触定义。鉴于结构形态及功能差异,理论上每个病患每次定制设计的产品均应进行单独的有限元分析计算。若结构形态按解剖部位与产品功能区进行了足够细分,可以设定计算边界,简化一定设计范围内不同产品之间的迭代计算。
4.个性化匹配植入物的有限元建模:
几何模型:应指出有限元分析所使用的骨及植入物的几何模型与原始设计模型之间的差异及其原因;
材料属性:应明确植入物材料性能及其来源,若植入物为非均质材料或包含多孔部分,需提供详细的各部位材料力学性能及其获取方式。随着功能区划分的不同,骨填充区和骨结合区的多孔结构力学性能参数、主应力区表面处理对材料力学性能的影响,都会影响有限元分析的建模,包括软组织力学参数设定,这些都应在有限元分析方案中特别界定;
边界条件:应根据骨植入物及周围骨在人体内的受力及约束情况为有限元模型施加边界条件,应指出边界条件与实际情况之间的差异及其合理性;
接触属性:骨植入物的有限元分析通常包含植入物和周围组织两个部分,根据策划文件中的植入物固定方案,在有限元模型中确定各个组件间的接触属性,并叙述其与植入物固定方案之间的关联;
载荷:根据植入物的使用环境,为有限元模型施加载荷,需明确载荷施加的方式及载荷类型、大小,并叙述其与植入物使用环境的关联。应明确植入物或工具最大应力的判定方法。在应力模型中明确所设置的受力点、载荷分布,应确保能使分析中产品所受应力风险“大于”所有可能的实际工况加载风险。应规定“大于”的程度,明确评估方法和指标,至少应包括对最大主应力、应变与位移的分析。模型修正与分析应明确静态与动态力学加载工况。静态应明确载荷加载点与约束部位,动态应明确步态、体态等运动状态载荷的变化及施力点;
单元类型和网格尺寸:应对模型的网格质量进行检查,避免网格划分的失真;应检查有限元模型的网格的收敛性。通过对同一模型不同网格密度的计算结果进行对比,证明所使用的网格密度的收敛性。如果运用了模型简化方法,应在建模前预先明确其合理性。网格划分应明确对几何自由边和硬点的清理规则,避免网格划分的失真。体单元网格质量应明确尺寸(长宽比、偏斜度、角度、雅可比,等等)和边界范围。规定产品与骨、产品组件间接触区域、孔、角、螺纹等局部特征的网格加密方式,网格收敛的应力变化限度。对多孔区与网格区的精细划分,建议运用对实物样件的X射线显微CT检测结果,保障模型仿真的准确性,与对孔隙结构缺陷的辨识。
5.有限元模型需经过验证才能证明其有效性,验证的方式包括常识性判断、与实际物理实验结果对比或与类似产品的研究报告对比等。有限元分析方案应根据计算精度设置计算时间步长,应经多次试算和两种以上方法进行结果评估,规定网格收敛性与应力集中的结果偏离限度,以及对调整模型参数与位移边界的限定。模型参数至少应包括单元数量、尺寸、材料属性。
6.有限元分析的结果,均应经所设计植入物或工具的动静态力学实测验证,所以应规定测试所需要的样本量。对耗时较长、可能延误定制产品及时交付使用的疲劳测试,应明确触发新的实际测试的条件,应明确既往经疲劳试验验证的有限元分析模型可涵盖的最大主应力、应变、位移、边界条件、应力/应变分布的范围。若新的个体化匹配产品设计突破此范围,应开展新的疲劳试验。
7.有限元分析的报告应按照预定的格式,按照上述要求叙述建模、验证过程及其合理性,并根据预期评价指标对分析结果进行呈现,呈现形式包括整体、组件和骨骼端的应力/应变分布变化云图、数值曲线等。
1.《医疗器械监督管理条例》(中华人民共和国国务院令第680号)
2.《医疗器械注册管理办法》(国家食品药品监督管理总局令第4号)
3.《医疗器械生产质量管理规范》(国家食品药品监督管理总局公告2014年第64号)
4.《无源植入性医疗器械产品注册申报资料指导原则》(食药监办械函[2009]519号)
5. YY/T 0316-2016《医疗器械风险管理对医疗器械的应用》
6. YY/T 0287-2017《医疗器械 质量管理体系 用于法规的要求》
附录:1.个性化匹配骨植入物及配套工具设计的通用流程
2.颌面(上颌、下颌)植入物及配套工具设计开发医工交互流程
3.颅(颅面、颅)植入物及配套工具设计开发医工交互流程
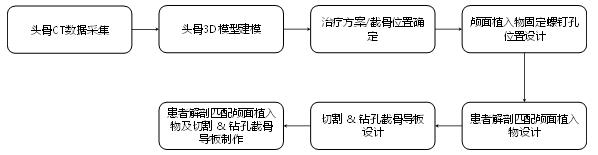
4.肩关节(肩胛骨、肱骨、锁骨)植入物及配套工具设计开发医工交互流程(需求到输入)
5.胸肋骨植入物及配套工具设计开发医工交互流程(需求到输入)
6.脊柱植入物及配套工具设计开发医工交互流程图(需求到输入)
7.骨盆植入物(非髋关节)及配套工具设计开发医工交互流程(需求到输入)
8.膝关节植入物及配套工具设计开发医工交互流程
9.髋关节植入物及配套工具设计开发医工交互流程
10.足踝关节植入物及配套工具设计开发医工交互流程图(需求到输入)
11.四肢创伤内固定植入物及配套工具设计开发医工交互流程图
附录1
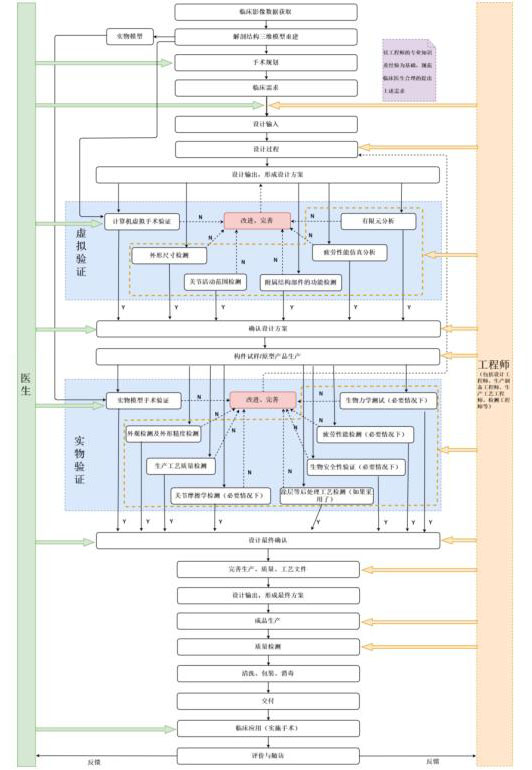
附录2
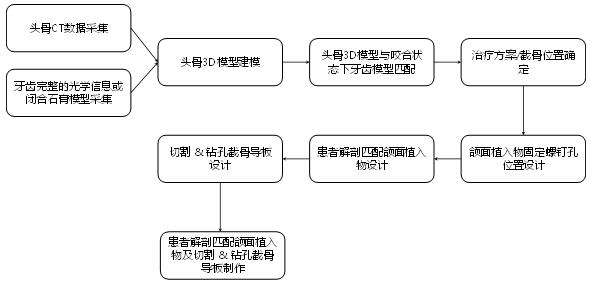
附录3
附录4
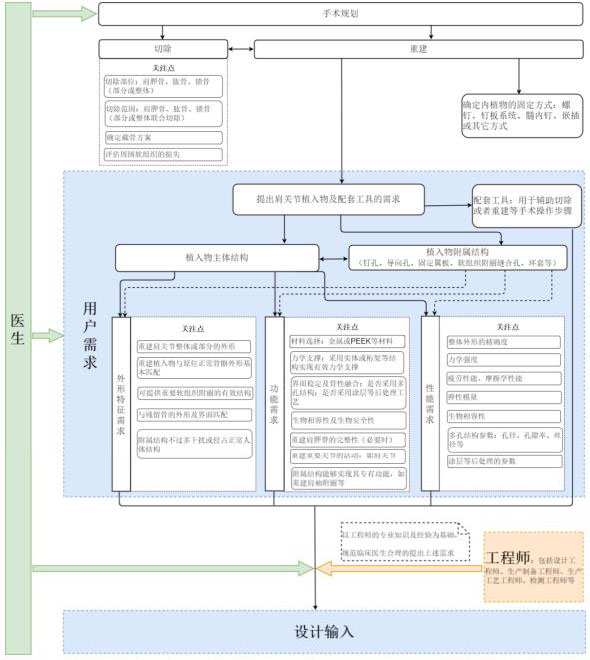
附录5
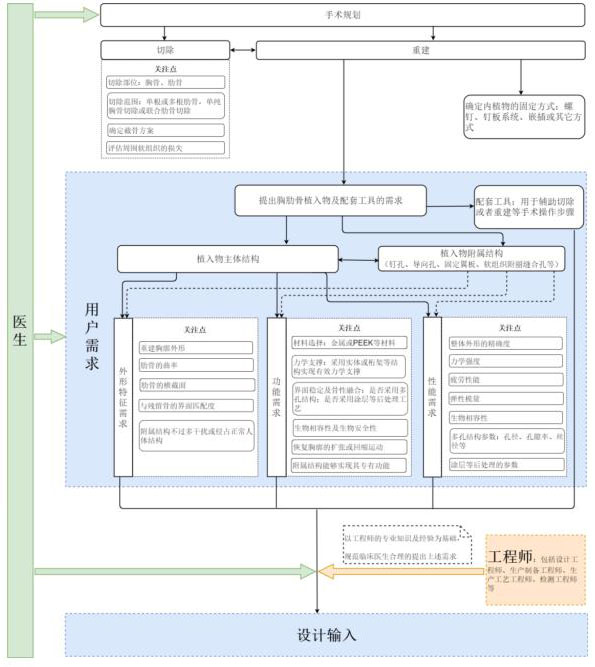
附录6
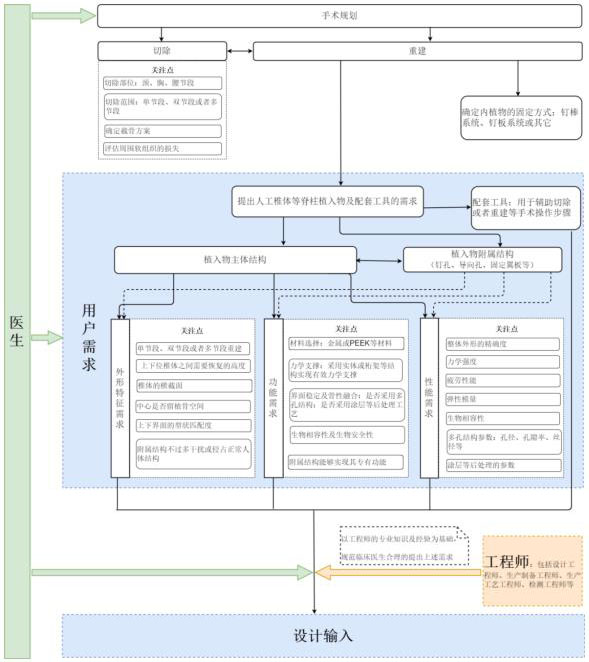
附录7
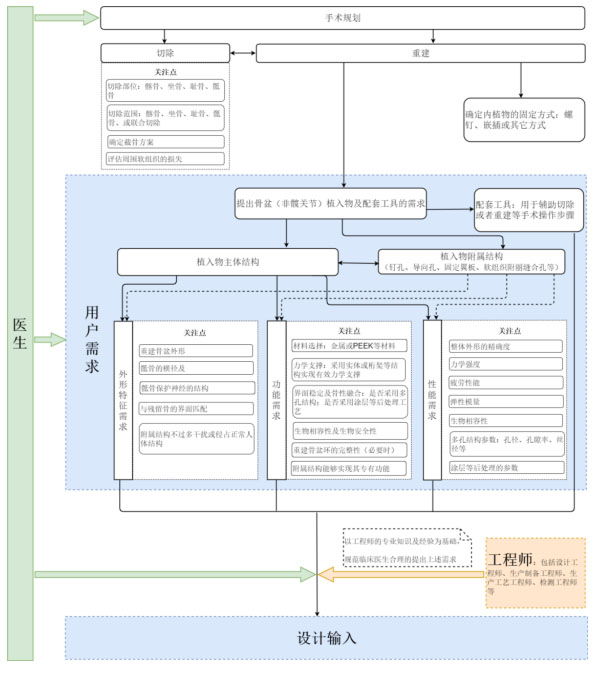
附录8
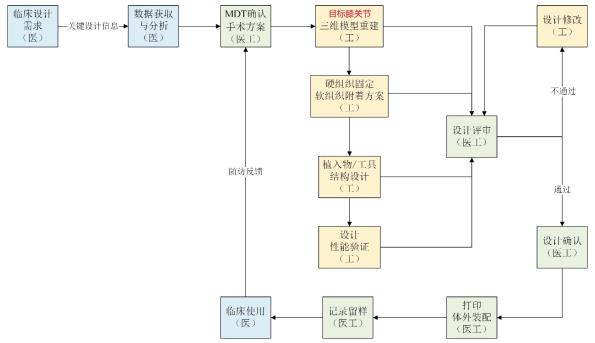
附录9
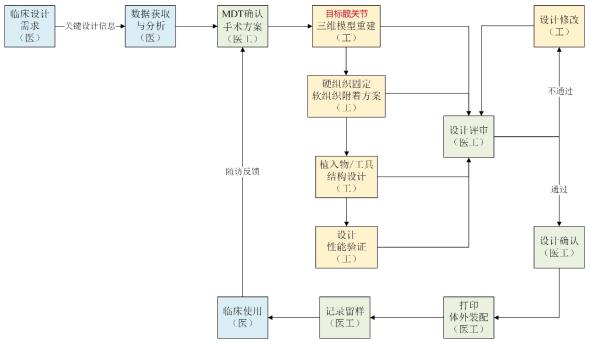
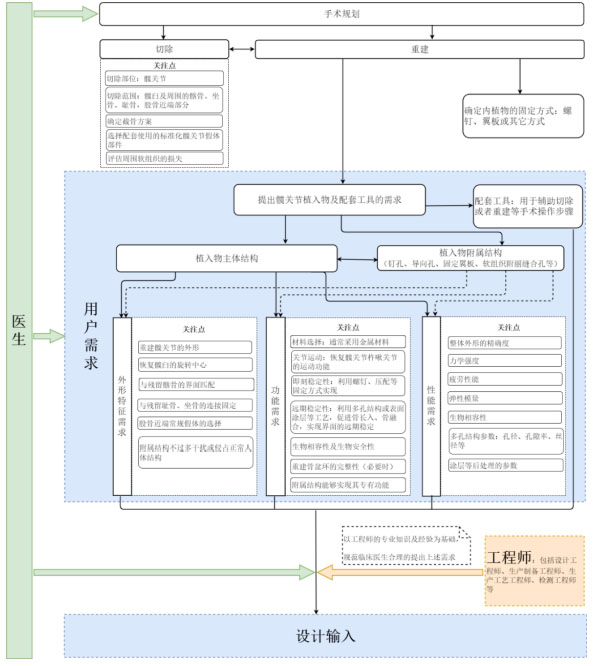
附录10
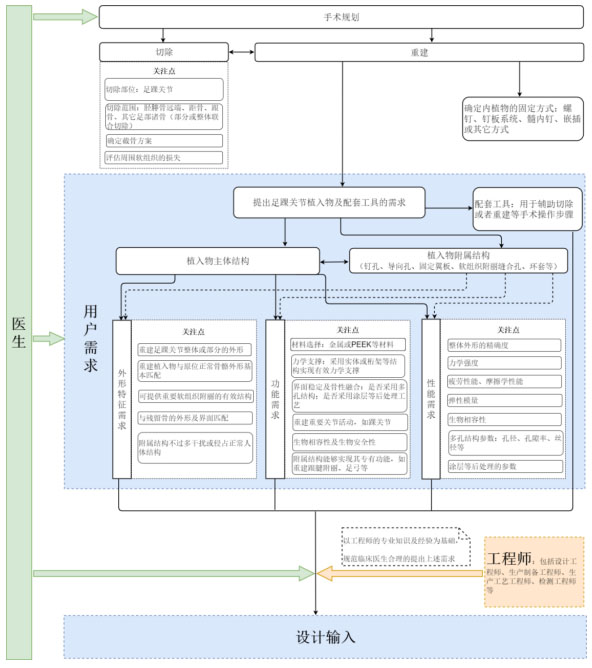
附录11

站点声明
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
思途医疗科技有限公司专注于医疗器械产品政策与法规规事务服务,提供产品注册备案申报代理、临床试验、体系建立辅导、分类界定、申请创新办理服务。
《海南博鳌乐城国际医疗旅游先行区医疗机构制剂调剂使用管理暂行办法》已经3月24日海南博鳌乐城国际医疗旅游先行区领导小组会议审议通过,现印发给你们,请遵照执行。

《海南博鳌乐城国际医疗旅游先行区临床急需进口药品带离先行区使用管理暂行办法》已经3月24日海南博鳌乐城国际医疗旅游先行区领导小组会议审议通过,现印发给你们,请遵照执行

为规范医疗器械注册人跨区域委托生产的监督管理,推进长江三角洲区域医疗器械跨区域监管,根据《中共中央办公厅国务院办公厅关于深化审评审批制度改革鼓励药品医疗器械创新的意见》《

附件:血液透析用水处理设备注册审查指导原则(2024年修订版)(2024年第19号).doc血液透析用水处理设备注册审查指导原则(2024年修订版)本指导原则旨在指导注册申请人对血液透析用水处理设备注册申报资料的准备及撰写,同时也为技术审评部门提供参考。本指导原则是对血液透析用水处理设备的一般要求,注册申请人依据产品的具体特性确定其中内容是否适用。若不适用,要具体阐述理由及相应的科学依据,并依据产

附件:一次性使用医用冲洗器产品注册审查指导原则(2022年第41号).doc一次性使用医用冲洗器产品注册审查指导原则本指导原则旨在指导注册申请人对一次性使用医用

本指导原则旨在帮助和指导注册申请人对一次性使用腹部穿刺器注册申报资料进行准备,以满足技术审评的基本要求。同时有助于审评机构对该类产品进行科学规范的审评,提高审评工

国家药监局器审中心关于发布影像型超声诊断设备(第三类)注册审查指导原则(2023年修订版)的通告(2024年第29号)发布时间:2024-10-14为进一步规范

附件:医用透明质酸钠创面敷料注册审查指导原则(2024年第21号).doc医用透明质酸钠创面敷料注册审查指导原则本指导原则旨在指导注册申请人准备及撰写医用透明质酸钠创面敷料注册申报资料,同时也为技术审评部门审查注册申报资料提供参考。本指导原则是对医用透明质酸钠创面敷料产品的一般要求,注册申请人应依据产品的具体特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对

附件:医用雾化器注册审查指导原则(2024修订版)(2024年第19号).doc 医用雾化器注册审查指导原则(2024年修订版) 本指导原则旨在指导注册申请人提交医用雾化器的注册申报资料,同时也为技术审评部门审查注册申报资料提供参考。 本指导原则是对医用雾化器的一般性要求,注册申请人应根据申报产品的特性提交注册申报资料,判断指导原则中的具体内容是否适用,不适用内容应阐述理

附件:重组胶原蛋白创面敷料注册审查指导原则(2023年第16号).doc重组胶原蛋白创面敷料注册审查指导原则本指导原则旨在指导注册申请人准备及撰写重组胶原蛋白创
六年
医疗器械服务经验
联系思途,免费获得专属《落地解决方案》及报价
咨询相关问题或咨询报价,可以直接与我们联系
思途CRO——医疗器械注册临床第三方平台