有源医疗器械加速老化试验效期验证及使用期限验证流程
为了确保医疗器械在生命周期内的安全及有效性,注册人应在设计开发中对其使用期限予以验证。使用期限的验证是医疗器械可靠性研究的重要组成部分,制定并验证合理的使用期限有
来源:医疗器械注册代办 发布日期:2024-12-05 阅读量:次

11月,国家药监局共42款医疗器械终止注册审查告知书送达信息,详情内容如下:
| 序号 | 受理号 | 产品名称 | 申请人 | 代理人 |
| 1 | CSY2400465 | B族链球菌抗原检测试剂盒(免疫层析法) | 广州华澳生物科技有限公司 | / |
| 2 | JSY2400809 | 抗链球菌溶血素O测定试剂盒(Latex比浊法) | 富士フィルム和光純薬株式会社 | 富士胶片和光纯耀(上海)化学有限公司 |
| 3 | CQY2400966 | 一次性使用医用连通器 | 深圳市昕力医疗设备开发有限公司 | / |
| 4 | CQZ2300909 | 口腔填充骨基质 | 上海亚朋生物技术有限公司 | / |
| 5 | CQZ2301153 | 牙种植体 | 北京市春立正达医疗器械股份有限公司 | / |
| 6 | CQZ2301929 | 远端通路导引导管 | 上海微密医疗科技有限公司 | / |
| 7 | CQZ2400455 | 椎体成形螺钉 | 常州集硕医疗器械有限公司 | / |
| 8 | CQZ2401599 | 血液/液体升温仪用一次性器械 | 杭州坦帕医疗科技有限公司 | / |
| 9 | CQZ2401655 | 一次性使用压力延长管 | 安徽百诺佳医疗科技有限公司 | / |
| 10 | JQZ2200130 | 纳米银抗菌敷料 | Smith & Nephew Medical Limited | 施乐辉医用产品国际贸易(上海)有限公司 |
| 11 | JQZ2300266 | 非球面丙烯酸酯人工晶状体 | HumanOptics Holding AG | 北京世代保康科技发展有限公司 |
| 12 | JQZ2300330 | 透析液过滤器 | 株式会社ジェイ・エム・エス | 新桥通科技(大连)有限公司 |
| 13 | JQZ2300430 | 可吸收界面螺钉 | Biomet Sports Medicine | 捷迈(上海)医疗国际贸易有限公司 |
| 14 | JQZ2400064 | 乳房旋切穿刺针 | Bard Peripheral Vascular, Inc. | 巴德医疗科技(上海)有限公司 |
| 15 | JQZ2400414 | 排龈线 | Sure Dent Corporation | 北京明光锐创医疗器械有限责任公司 |
| 16 | JQZ2400440 | 天然橡胶胶乳男用避孕套 | Karex Industries Sdn. Bhd. | 广州超鸟健康产业科技有限公司 |
| 17 | JQX2301264 | 双氧护理液 | Alcon Laboratories, Incorporated | 爱尔康(中国)眼科产品有限公司 |
| 18 | CQX2401616 | 一次性使用自损毁型无菌注射器 | 江西青山堂医疗器械有限公司 | / |
| 19 | JQX2401470 | 灌注泵 | Biosense Webster (Israel) Ltd. | 强生(上海)医疗器材有限公司 |
| 20 | JQX2401473 | 牙科影像版扫描仪 | PaloDEx Group Oy | 盈纬达(上海)医疗器械有限公司 |
| 21 | CQZ2200729 | 深冻异体皮 | 江西省科星生物工程有限公司 | / |
| 22 | CQZ2301027 | 妇科用人源化胶原蛋白 | 山西锦波生物医药股份有限公司 | / |
| 23 | CQZ2301080 | 脊柱内固定系统 | 北京市春立正达医疗器械股份有限公司 | / |
| 24 | CQZ2301092 | 髋关节假体-组配式翻修型股骨柄 | 北京市春立正达医疗器械股份有限公司 | / |
| 25 | CQZ2301332 | 胶原蛋白软骨再生载体 | 康膝生物医疗(深圳)有限公司 | / |
| 26 | CQZ2302300 | 一次性使用无菌胰岛素注射器 | 常州医疗器材总厂股份有限公司 | / |
| 27 | CQZ2400145 | 泪道引流管 | 山东史蒂夫医疗科技有限公司 | / |
| 28 | CQZ2300806 | 麻醉深度监护仪 | 深圳市美的连医疗电子股份有限公司 | / |
| 29 | CSZ2300208 | 人肿瘤多基因检测试剂盒(联合探针锚定聚合测序法) | 苏州吉因加生物医学工程有限公司 | / |
| 30 | CSZ2300225 | 多项毒品联合检测试剂盒(胶体金法) | 上海八通生物科技股份有限公司 | / |
| 31 | CSZ2400104 | 人类SLCO1B1、APOE基因多态性检测试剂盒(荧光 PCR 法) | 江苏百世诺医疗科技有限公司 | / |
| 32 | CSZ2400107 | 人类ACE、ADRB1、CYP2C9、CYP2D6基因多态性检测试剂盒(荧光PCR法) | 江苏百世诺医疗科技有限公司 | / |
| 33 | JSZ2200020 | 乙型肝炎病毒表面抗原(HBsAg)确认试剂 | Fujirebio Inc. | / |
| 34 | JSZ2200044 | 果糖胺测定试剂盒(四氮唑蓝法) | SENTINEL CH. S.p.A. | / |
| 35 | CQX2401606 | 脊柱后路内固定系统 | 山东威高骨科材料股份有限公司 | / |
| 36 | CQX2401638 | 富血小板血浆制备用套装 | 厦门博森再生医学工程有限公司 | / |
| 37 | CQY2401036 | 密闭式防针刺伤型静脉留置针 | 广东百合医疗科技股份有限公司 | / |
| 38 | CQZ2401876 | 口腔颌面锥形束计算机体层摄影设备 | 四川乃康科技有限公司 | / |
| 39 | CSZ2200258 | 血小板抗体检测试剂 | 江苏力博医药生物技术股份有限公司 | / |
| 40 | CSZ2300248 | 人疱疹病毒6型核酸检测试剂盒(PCR-荧光探针法) | 湖北朗德医疗科技有限公司 | / |
| 41 | JQZ2300559 | 射频微针电极 | Jeisys Medical Inc. | 北京迈锐思商贸有限公司 |
| 42 | JQZ2300320 | 囊胚序贯培养液 | ORIGIO a/s 澳励晶 | 库博医疗科技(上海)有限公司 |
文章来源:国家药品监督管理局

站点声明
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
思途医疗科技有限公司专注于医疗器械产品政策与法规规事务服务,提供产品注册备案申报代理、临床试验、体系建立辅导、分类界定、申请创新办理服务。
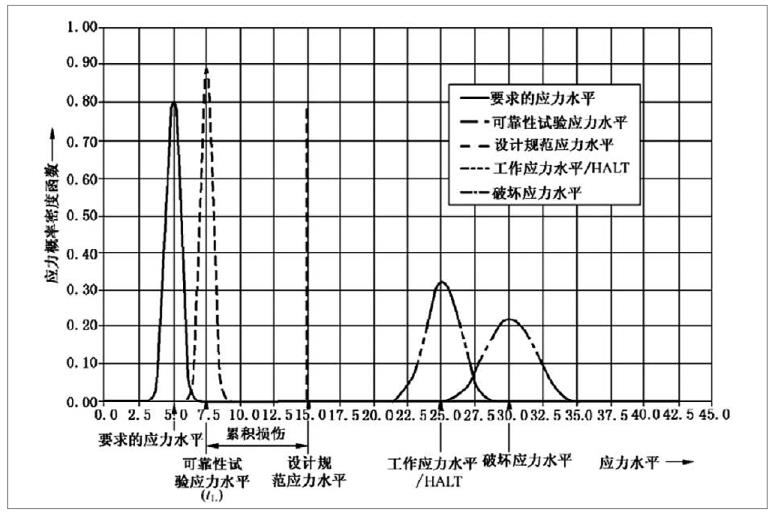
为了确保医疗器械在生命周期内的安全及有效性,注册人应在设计开发中对其使用期限予以验证。使用期限的验证是医疗器械可靠性研究的重要组成部分,制定并验证合理的使用期限有

润滑剂类产品在美国根据产品预期用途的不同主要分为人体润滑剂和患者润滑剂:其中,人体润滑剂主要成分为水、丙二醇、羟乙基纤维素、苯甲酸、卡波姆、氢氧化钠等,作用于生殖

中国能排进世界十大医疗器械制造强国吗?暂时还不能,因为排进前十的国家都有许多知名械企和世界级医疗器械巨头;而中国比较出名的可能只有迈瑞了,其他械企仍需努力了。下面

本文介绍了欧盟医疗器械新法规MDR相比于将替代的MDD法规的几点新增要求。建议收藏学习。明年5月份起,Medical Devices Regulation(MDR)(2017/745/ EU)将替代原本的Medical Devices Directive (93
可吸收高分子材料介绍,及其在植入医疗器械中的应用。1、植入产品的定义国家食品药品监督管理局《医疗器械分类规则》(局令第15号)第八条中对“植入器械”的定义为:任何借助

生物材料在疾病治疗和医疗保健中发挥了重要的作用,按材料性质,生物材料可分为惰性材料与可降解性材料两种,目前生物材料的发展呈现出由惰性向可降解性(水解和酶降解)转变的趋

医疗器械注册费是行政性收费,按照注册单元收取,部分省份不收取医疗器械注册费用,绝大部分省份还是收取的。本篇文章统计了截止到2022年1月5日各地医疗器械注册收费标准。

一个产品带有CE 标志(标记) 也就意味着其制造商宣告:该产品符合欧洲的健康、安全、与环境保护之相关法律中所规定 的基本要求。因而该产品是对:使用者(译者注:人)、宠物(

2021年2月5日,湖南省药监局分别与湖南省计量检测研究院、湖南新领航检测技术有限公司、湖南普瑞玛药物研究中心有限公司、深圳华通威国际检验有限公司、南德认证检测(中国)有限公
为服务中国(广东)自由贸易试验区和科创中心国家战略,全面贯彻党的十九大精神和总书记对广东重要指示批示精神,深化供给侧结构性改革,建设健康中国,奋力实现“四个走在全
六年
医疗器械服务经验
联系思途,免费获得专属《落地解决方案》及报价
咨询相关问题或咨询报价,可以直接与我们联系
思途CRO——医疗器械注册临床第三方平台