「CRC经验总结」SAE上报中的一些注意事项
在过去几年的工作中,我发现SAE上报既是临床试验工作中的重点难点,也是CRC工作中的痛点。当你是小白时,看到SAE就很头大,天然地产生一种畏惧心理,谈SAE色变,当你经验比较丰富
来源:医疗器械注册代办 发布日期:2024-09-13 阅读量:次
在临床试验中,不良事件(Adverse Event, AE)的监测和评估是确保受试者安全的重要环节。为了更好地理解和管理AE,通常会对AE进行分级,并根据一定的标准来判定AE的发生。本文将详细介绍AE的分级及判定依据。

AE可以根据其严重程度分为不同的等级,常见的分级方式有两种:
这种分级方式较为直观,适用于一般情况下的不良事件分类。轻度AE指的是对受试者日常生活影响较小,无需特殊处理或仅需简单处理即可恢复的不良事件;中度AE则是指需要采取一定的医疗干预措施才能缓解的不良事件;重度AE则是指对受试者健康构成严重威胁,需要紧急处理的不良事件。
NCI-CTC(美国国立癌症研究所-常见毒性标准)是一种更为详细的AE分级标准,常用于癌症临床试验中。根据这一标准,AE被划分为五个等级:
1级(轻微):不良事件存在但对受试者日常生活影响不大,一般不需要特殊处理。
2级(中度):不良事件对受试者日常生活有一定影响,需要采取一定的医疗干预措施。
3级(重度):不良事件严重影响受试者日常生活,需要立即采取医疗措施。
4级(危及生命):不良事件危及受试者生命安全,需要紧急处理。
5级(致命):不良事件直接导致受试者死亡。
判定AE的依据主要包括以下几个方面:
如果受试者在试验过程中原有的症状或体征有所加剧,例如头痛加剧、恶心呕吐频率增加等,这些变化都可能被视为AE的表现。
如果在试验过程中出现了新的疾病诊断,比如感染性疾病、心血管事件等,这些新发疾病也可能被归类为AE。
通过实验室检查发现的异常结果,如血液生化指标异常、血细胞计数异常等,这些异常结果如果与受试者在接受试验药物后的生理变化相关,也可能被判定为AE。
受试者在试验过程中出现的任何新的不适症状,如皮疹、肌肉疼痛等,都应被记录并评估是否为AE。
AE的分级和判定是临床试验中非常重要的环节,它直接关系到受试者的安全和试验数据的可靠性。通过对AE进行科学的分级,并依据原有症状、体征的加重、新诊断的疾病、实验室异常值及新出现的症状来判定AE,可以更准确地评估药物的安全性,为受试者的健康提供保障。希望本文能够帮助读者更好地理解AE分级及判定的依据,从而在临床试验中更加科学地管理和应对AE。

站点声明
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
思途医疗科技有限公司专注于医疗器械产品政策与法规规事务服务,提供产品注册备案申报代理、临床试验、体系建立辅导、分类界定、申请创新办理服务。

在过去几年的工作中,我发现SAE上报既是临床试验工作中的重点难点,也是CRC工作中的痛点。当你是小白时,看到SAE就很头大,天然地产生一种畏惧心理,谈SAE色变,当你经验比较丰富

新版GCP的SAE/SUSAR怎么上报?先来了解一下什么是SAE?什么是SUSAR?跟随小编的脚步一起看看SAE和SUSAR的关系,最后再来探讨上报。正文如下:

根据《中华人民共和国传染病防治法》第七十八条的规定,消毒是指用化学、物理、生物的方法杀灭或者消除环境中的病原微生物。 在作用目的上,它是一种防病的产品,而不是

不良事件相关性判定,基于什么原则来考虑?参考研究者手册?去激发、再激发?七分、六分、五分、二分...为什么相关性判定的分级方式不同, 哪一种才是权威的?众多相关性判定方
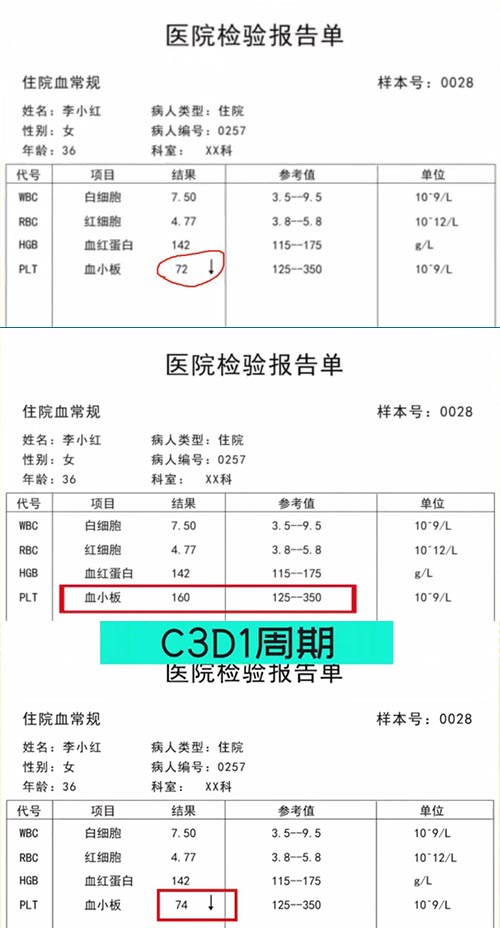
某乳腺癌项目012号受试者,基线期血小板计数降低II级,研究者判断有临床意义,并将血小板计数降低记录在病史之中。C2D15周期用药前实验室检查显示恢复了正常水平,然后在C3D1周期用
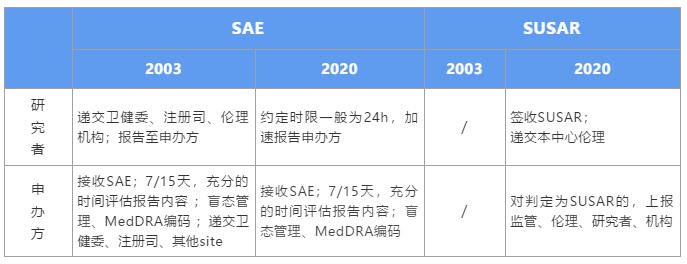
新版GCP对于申办方的影响是全方位的,就SAE个例报告处理方面,强化了申办方的主体责任,细化了申办方对SAE的管理流程。在此,我们详细解读,在新规之下,该如何高效、合规的处理

医疗器械注册检验的依据,业内应该都比较统一,如果是第一次接触还真不知道是什么?一起来看看依据的哪个法规。医疗器械注册检验的依据是什么?抗HPV妇科凝胶在医院销量特别好

不管是在中国还是国外,都有方案将AE的开始收集时间定义为签署ICF之后就开始收集,而不是等到首次研究治疗/干预/用药。根据检索相关信息,这一设定的考量可能包括以下几点(从临

上期分享了CRC在临床启动会中文件签署不全或丢失的处理方法,本期为了平衡CRC的感受......哈哈,我们研究一下CRA监查时偶遇问题,在惬意的假期时光,抽出宝贵的两分钟,来温习一个
在众志成城,共克时艰,全国人民携手抗击新冠肺炎疫情的时候,临床试验领域也面临着诸多挑战!为了保证疫情防控下的受试者安全,各医疗机构和申办方/CRO都对临床试验工作的有序
六年
医疗器械服务经验
联系思途,免费获得专属《落地解决方案》及报价
咨询相关问题或咨询报价,可以直接与我们联系
思途CRO——医疗器械注册临床第三方平台