赫尔辛基宣言(2024版)
2024年10月19日,在第 75 届世界医学会全体大会上正式通过了《赫尔辛基宣言》的最新修订版本;《赫尔辛基宣言》作为人类参与者的医学研究伦理
来源:医疗器械注册代办 发布日期:2024-05-11 阅读量:次
本程序适用于日常监管、稽查、投诉举报、信访、行政执法、刑事司法、法院案件等工作中涉及需要确认产品管理属性或者管理类别的特殊情形。特殊情形分类界定程序不在分类界定信息系统中办理。
由所在地市级负责药品监督管理的部门或者省级药品监督管理部门依据《条例》《分类规则》、相关产品分类界定指导原则及《分类目录》等,结合产品实际情况作出判定。必要时,下级药品监督管理部门可以向上一级药品监督管理部门提出请示,并提供用于支持产品属性判定及分类界定的相应资料及明确的管理属性及管理类别意见。
国家药监局遇有本程序所适用情形时,由相关司局组织器械标管中心研究确定。
器械标管中心根据来函及相应产品资料,研究确定产品管理属性和类别。对于所附资料过少、难以判断产品管理属性和管理类别的,可请来函单位进一步提供资料;对于分类界定难度大、技术复杂、存在异议的产品,器械标管中心可以组织专家会议研究。
对于上述事项,根据来函及相应产品资料,能够明确产品管理属性和类别意见的,应当提供产品管理属性及分类界定意见;提供的产品资料不全面、无法明确产品管理属性和类别意见的,可以视资料情况只提供该产品是否作为医疗器械管理、第一类或者不低于二类的分类界定意见,或者提供相关产品管理属性及分类判定的原则,供来函单位根据具体情况进行研判或参考。
管理属性及分类意见系依据来函所附产品资料作出,若后续提供的产品相关内容与来函所附产品资料不一致,则原管理属性及分类意见不适用。

站点声明
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
思途医疗科技有限公司专注于医疗器械产品政策与法规规事务服务,提供产品注册备案申报代理、临床试验、体系建立辅导、分类界定、申请创新办理服务。

2024年10月19日,在第 75 届世界医学会全体大会上正式通过了《赫尔辛基宣言》的最新修订版本;《赫尔辛基宣言》作为人类参与者的医学研究伦理

附件:血液透析用水处理设备注册审查指导原则(2024年修订版)(2024年第19号).doc血液透析用水处理设备注册审查指导原则(2024年修订版)本指导原则旨在指导注册申请人对血液透析用水处理设备注册申报资料的准备及撰写,同时也为技术审评部门提供参考。本指导原则是对血液透析用水处理设备的一般要求,注册申请人依据产品的具体特性确定其中内容是否适用。若不适用,要具体阐述理由及相应的科学依据,并依据产

国家药监局器审中心关于发布影像型超声诊断设备(第三类)注册审查指导原则(2023年修订版)的通告(2024年第29号)发布时间:2024-10-14为进一步规范

附件:医用透明质酸钠创面敷料注册审查指导原则(2024年第21号).doc医用透明质酸钠创面敷料注册审查指导原则本指导原则旨在指导注册申请人准备及撰写医用透明质酸钠创面敷料注册申报资料,同时也为技术审评部门审查注册申报资料提供参考。本指导原则是对医用透明质酸钠创面敷料产品的一般要求,注册申请人应依据产品的具体特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对

附件:医用雾化器注册审查指导原则(2024修订版)(2024年第19号).doc 医用雾化器注册审查指导原则(2024年修订版) 本指导原则旨在指导注册申请人提交医用雾化器的注册申报资料,同时也为技术审评部门审查注册申报资料提供参考。 本指导原则是对医用雾化器的一般性要求,注册申请人应根据申报产品的特性提交注册申报资料,判断指导原则中的具体内容是否适用,不适用内容应阐述理

附件:康复类数字疗法软件产品分类界定指导原则(2025年第27号).doc康复类数字疗法软件产品分类界定指导原则一、目的为指导康复类数字疗法软件产品管理属性和管

国家药监局药审中心关于发布《抗肿瘤药物临床试验中SUSAR分析与处理技术指导原则》的通告(2024年第42号) 发布日期:20241010

附件:医学图像存储与传输软件(PACS)注册审查指导原则(2024年修订版)(2024年第19号).doc 医学图像存储与传输软件(PACS)注册审查指导原则(2024年修订版) 本指导原则旨在指导注册申请人对医学图像存储与传输软件(PACS)注册申报资料的准备及撰写,同时也为技术审评部门提供参考。 本指导原则是对医学图像存储与传输软件(PACS)的一般要求,注册申请人应
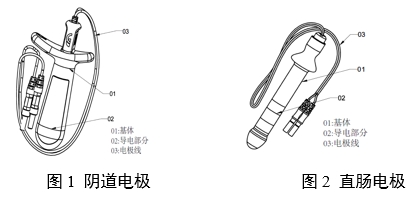
附件:神经和肌肉刺激器用体内电极注册审查指导原则(2024年第19号).doc神经和肌肉刺激器用体内电极注册审查指导原则本指导原则旨在指导注册申请人对神经和肌肉刺激器用体内电极(以下简称刺激器用体内电极)注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。本指导原则是对刺激器用体内电极注册申报资料的一般要求,申请人应依据产品的具体特性确定其中的内容是否适用。若不适用,需具体阐述

附件:一次性使用引流管产品注册审查指导原则(2024年修订版)(2024年第21号).doc一次性使用引流管产品注册审查指导原则(2024年修订)本指导原则旨在帮助和指导注册申请人对一次性使用引流管注册申报资料的准备及撰写,同时也为医疗器械技术审评部门对注册申报资料的技术审评提供参考。本指导原则是对一次性使用引流管注册申报资料的一般要求,注册申请人应依据具体产品的特性对注册申报资料的内容进行充分说
六年
医疗器械服务经验
联系思途,免费获得专属《落地解决方案》及报价
咨询相关问题或咨询报价,可以直接与我们联系
思途CRO——医疗器械注册临床第三方平台