山东省医疗器械工艺用水现场检查指南(鲁药监械〔2021〕35号)
为规范医疗器械现场检查,提升检查员现场检查能力,指导检查员对医疗器械生产企业工艺用水控制情况的检查,提高企业工艺用水质量安全保证水平,依据《医疗器械监督管理条例》
来源:医疗器械注册代办 发布日期:2024-01-25 阅读量:次

(2024年第1号)
发布时间:2024-01-25
为加强药物临床试验机构监督管理,规范年度工作总结报告的撰写工作,国家药品监督管理局食品药品审核查验中心组织制定了《药物临床试验机构年度工作总结报告填报指南》(见附件),经国家药品监督管理局同意,现予发布。
特此通告。
国家药品监督管理局食品药品审核查验中心
2024年1月25日
附件
本指南旨在为药物临床试验机构在“药物临床试验机构备案管理信息平台”上提交药物临床试验机构年度工作总结报告(以下简称“年度报告”)提供指导,并提出撰写和提交年度报告时需要考虑的要点。本指南中药物临床试验是指以药品上市注册为目的,按照《中华人民共和国药品管理法》《药品注册管理办法》等有关规定开展的药物临床试验。
根据《中华人民共和国药品管理法》《药品注册管理办法》规定,药物临床试验应当在具备相应条件并按规定备案的药物临床试验机构开展。2019年12月1日,《药物临床试验机构管理规定》开始施行,“药物临床试验机构备案管理信息平台”同时上线。根据《药物临床试验机构管理规定》要求,药物临床试验机构应当于每年1月31日前在备案平台填报上一年度开展药物临床试验工作总结报告。
为统一年度报告填报格式,规范填报内容,保证填报质量,为临床试验监督管理提供客观、准确、高质量数据,核查中心在总结了既往工作经验的基础上,起草了本指南,用于已备案的机构在备案平台上填报年度报告,以明确撰写和提交年度报告时需要考虑的要点。
年度报告的主要目的是对上一年度机构开展药物临床试验的相关工作进行全面深入系统的总结。内容应从组织管理体系建设、人员培训情况、文件体系变更情况、质量控制实施情况、伦理委员会、接受境内外检查情况及下一年度计划等七个方面阐述。
年度报告应简明扼要、重点突出。机构应保证所提供的信息真实准确,能涵盖上一年度药物临床试验相关的所有工作,确保能够根据年度报告对机构工作进行掌握和评估。
年度报告的数据收集周期应为上一公历年的第一天至最后一天。如为新备案机构,则年度报告的数据收集起始日期为备案成功取得备案号的日期,如,机构备案时间为5月1日,则第一次提交年度报告的时间应为第二年1月31日前。
本节中所包含内容在年度报告中均应有所体现,如没有相关信息应加以说明。
(一)组织管理体系建设
本部分应当显示上一年度机构关键信息重要变更情况以及开展药物临床试验项目情况,主要内容包括:
1. 应列出机构基本信息的重要变更:
机构名称是否发生变更,如有,列出变更前后的信息;
机构法人是否发生变更,如有,列出变更前后的信息;
机构地址是否发生变更,如有,列出变更前后的信息;
机构负责人是否发生变更,如有,列出变更前后的信息;
临床试验管理部门负责人是否发生变更,如有,列出变更前后的信息;
联系人及联系方式是否发生变更,如有,列出变更前后的信息;
2. 列表说明备案专业/试验现场的变更情况,列出新增、取消或变更地址的专业/试验现场;对新增专业/试验现场的自评估情况进行概述。
3. 列表说明主要研究者的变更情况,分专业列出主要研究者的新增或取消的情况;说明新增主要研究者参加3个药物临床试验的情况。
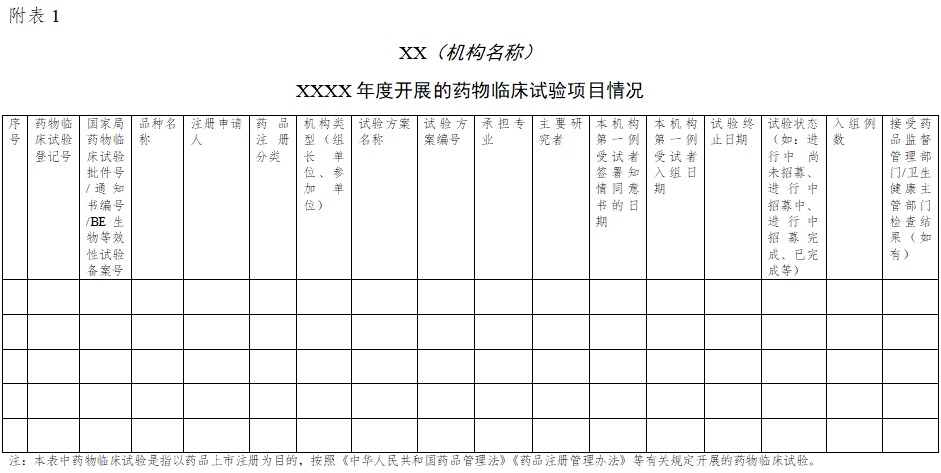
4. 应通过表格的方式总结上一年度开展的药物临床试验项目情况(包括上一年度启动和完成项目,以及其他在研项目),收集数据截止时间为上一年的12月31日,主要内容如下:
明确试验基本信息,包括品种名称、注册申请人、药品注册分类、机构类型(明确本机构为组长单位或参加单位)、药物临床试验登记号、国家局药物临床试验批件号/通知书编号/生物等效性试验备案号、试验方案名称、试验方案编号;
明确关键时间节点,包括本机构第一例受试者签署知情同意书的日期、第一例受试者入组日期和试验终止日期;
明确承担试验的专业及主要研究者;
明确试验状态以及入组例数。
如试验接受了药品监督管理部门/卫生健康主管部门检查,需填写检查结果。
(二)人员培训情况
本部分应总结上一年度本机构组织培训情况,主要内容包括:
1. 总结上一年度本机构组织培训的总人次;组织管理机构工作人员、研究人员、质量管理人员、药品管理人员、伦理委员、CRC参加培训的人次。
2. 各类培训开展情况应列表,内容包括培训名称、培训类别(如法规、专业技能等)、培训涉及部门、参加培训人次、培训考核情况(如有)。
(三)文件体系变更情况
本部分应使用表格形式列出文件体系变更,包括文件名称、类别(制度、SOP)、变更前和变更后文件名,如变更前和变更后文件名称相同,可填写版本号及版本日期以示区别;简要描述变更的内容和理由。
(四)质量控制实施情况
本部分应列出上一年度机构质量控制的实施情况,主要内容包括:
1. 质控实施项目数、质控实施项目数占总项目数的百分比、质控实施总次数。
2. 说明机构对主要研究者的临床试验管理效能与其承担试验项目类型和数量、参加研究人员数量和经验、受试者人群类型和数量等进行匹配度分析的情况(如采取的评估方式、评估结果等),以及机构相应的质量管理措施。
3. 简要描述质控发现的主要问题和处理情况,包括风险评估、风险控制、改进措施等。
(五)伦理委员会
本部分应当显示上一年度伦理委员会重要变更及开展审查情况,主要内容包括:
1. 主任委员是否变更,如有,列出变更前后的信息;
2. 委员是否换届,如有,列出换届前后委员名单;
3. 是否新增通过伦理认证的情况,如有,应说明通过的认证名称和通过认证的时间;
4. 年度审查项目数量,写明年度审查药物临床试验项目的总数量,并列出初始审查和跟踪审查的项目数量,以及快审和会议审查的项目数量;
5. 简述年度伦理审查发现的问题和处理情况。
(六)接受境内外检查情况
本部分应阐述上一年度本机构接受境内外检查的情况,主要内容包括:
1. 如接受过国内药品监管部门检查,需填写检查次数,并使用表格形式列出接受检查情况,包括监管机构、检查类型(包括首次监督检查、日常监督检查、有因检查、药品注册核查、其他检查等)、检查日期、检查结论以及是否针对检查发现问题完成整改,如有未完成整改的,说明原因。
2. 如接受过境外药品监管部门检查,需填写检查次数,并使用表格形式列出接受检查情况,包括监管机构、检查日期、检查中发现的主要问题、检查结论以及是否针对检查发现问题完成整改,如有未完成整改的,说明原因。
(七)下一年度计划
简要叙述下一年度将针对药物临床试验机构管理的哪些方面进行加强或改善。







站点声明
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
思途医疗科技有限公司专注于医疗器械产品政策与法规规事务服务,提供产品注册备案申报代理、临床试验、体系建立辅导、分类界定、申请创新办理服务。
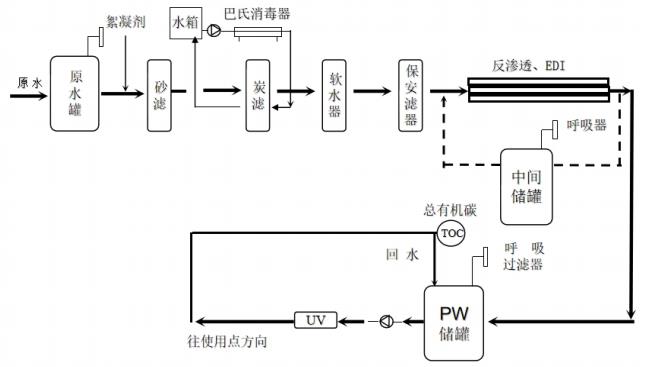
为规范医疗器械现场检查,提升检查员现场检查能力,指导检查员对医疗器械生产企业工艺用水控制情况的检查,提高企业工艺用水质量安全保证水平,依据《医疗器械监督管理条例》

《海南博鳌乐城国际医疗旅游先行区临床急需进口药品带离先行区使用管理暂行办法》已经3月24日海南博鳌乐城国际医疗旅游先行区领导小组会议审议通过,现印发给你们,请遵照执行

2024年10月19日,在第 75 届世界医学会全体大会上正式通过了《赫尔辛基宣言》的最新修订版本;《赫尔辛基宣言》作为人类参与者的医学研究伦理

附件:血液透析用水处理设备注册审查指导原则(2024年修订版)(2024年第19号).doc血液透析用水处理设备注册审查指导原则(2024年修订版)本指导原则旨在指导注册申请人对血液透析用水处理设备注册申报资料的准备及撰写,同时也为技术审评部门提供参考。本指导原则是对血液透析用水处理设备的一般要求,注册申请人依据产品的具体特性确定其中内容是否适用。若不适用,要具体阐述理由及相应的科学依据,并依据产

国家药监局关于发布免于进行临床评价医疗器械目录的通告(2025年第19号)发布时间:2025-05-13为做好医疗器械注册管理工作,根据《医疗器械注册与备案管理

关于发布医疗器械质量管理体系年度自查报告编写指南的通告(2022年第13号)发布时间:2022-03-24为加强医疗器械生产监管,保障医疗器械安全有效,根据《医

国家药监局器审中心关于发布影像型超声诊断设备(第三类)注册审查指导原则(2023年修订版)的通告(2024年第29号)发布时间:2024-10-14为进一步规范

附件:医用透明质酸钠创面敷料注册审查指导原则(2024年第21号).doc医用透明质酸钠创面敷料注册审查指导原则本指导原则旨在指导注册申请人准备及撰写医用透明质酸钠创面敷料注册申报资料,同时也为技术审评部门审查注册申报资料提供参考。本指导原则是对医用透明质酸钠创面敷料产品的一般要求,注册申请人应依据产品的具体特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对

附件:医用雾化器注册审查指导原则(2024修订版)(2024年第19号).doc 医用雾化器注册审查指导原则(2024年修订版) 本指导原则旨在指导注册申请人提交医用雾化器的注册申报资料,同时也为技术审评部门审查注册申报资料提供参考。 本指导原则是对医用雾化器的一般性要求,注册申请人应根据申报产品的特性提交注册申报资料,判断指导原则中的具体内容是否适用,不适用内容应阐述理

国家药监局药审中心关于发布《抗肿瘤药物临床试验中SUSAR分析与处理技术指导原则》的通告(2024年第42号) 发布日期:20241010
六年
医疗器械服务经验
联系思途,免费获得专属《落地解决方案》及报价
咨询相关问题或咨询报价,可以直接与我们联系
思途CRO——医疗器械注册临床第三方平台