有源医疗器械加速老化试验效期验证及使用期限验证流程
为了确保医疗器械在生命周期内的安全及有效性,注册人应在设计开发中对其使用期限予以验证。使用期限的验证是医疗器械可靠性研究的重要组成部分,制定并验证合理的使用期限有
来源:医疗器械注册代办 发布日期:2022-04-22 阅读量:次
阿尔茨海默症(AD)是一种起病隐匿的进行性发展的神经系统退行性疾病。临床上以记忆障碍、失语、失用、失认、视空间技能损害、执行功能障碍以及人格和行为改变等全面性痴呆表现为特征,病因迄今未明。65岁以前发病者,称早老性痴呆;65岁以后发病者称老年性痴呆。
阿兹海默症是困扰全球的一大疾病。据估计,到2050年,仅在美国,就将有1400万人生活在阿兹海默症的阴影之下。作为全球第六大死因,阿兹海默症每年造成了数十亿美元的医疗支出。

在这两项临床试验中,研究人员们专注的新药叫做aducanumab,它基于的是“淀粉样蛋白假说”。尽管之前所有针对这一靶点的新药都在临床试验中折戟沉沙,但Biogen的研究人员们依然决定推进这一疗法的研发。他们希望能够通过预防淀粉样蛋白的沉积,起到改善认知和运动能力的效果。
2017年,在一项大型的1期临床试验中,研究人员们看到了积极的迹象。他们发现,随着剂量的上升,患者脑中的淀粉样蛋白沉积随之下降。以此为基点,研究人员们决定启动两项大型的3期临床试验ENGAGE与EMERGE。而他们要挑战的是一座险峰——证实药物对认知能力有改善,且不会有危险的副作用。
去年2月,Biogen宣布将招募额外500名患者进行评估,让人们一度对这两项研究的前景产生了担忧。而由于患者招募规模的扩大,这两项研究的结果可能要到2019年末,乃至2020年才会得到揭晓。无论结果如何,这款新药的成绩都会在业内带来重要的影响。

站点声明
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
思途医疗科技有限公司专注于医疗器械产品政策与法规规事务服务,提供产品注册备案申报代理、临床试验、体系建立辅导、分类界定、申请创新办理服务。
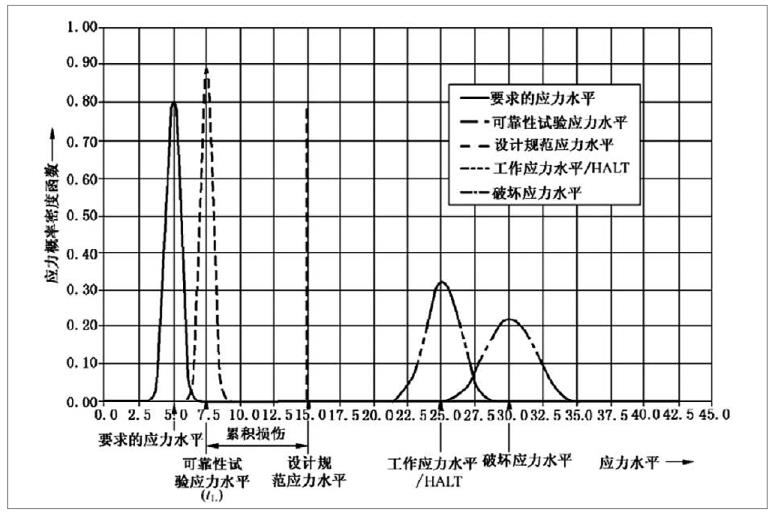
为了确保医疗器械在生命周期内的安全及有效性,注册人应在设计开发中对其使用期限予以验证。使用期限的验证是医疗器械可靠性研究的重要组成部分,制定并验证合理的使用期限有

简述了中药新药临床试验主要特点,指出要重视风险、受益评估,重视人 用经验选择科学、客观、合适的有效性指标,做好中医证候疗效评价,鼓励在中药新药临床研究中采用电子化手

近日美国食品药品监督管理局(FDA)更新了《医疗器械提交的反馈申请和会议申请:Q-Submission指导原则》。此文件是对2019版Q-sub指导原则的更新,更新的主要内容如下:1. 增加了STeP医疗

低频脉冲电刺激作为一种新型的物理治疗手段逐渐被人们所关注,神经的活动(兴奋、抑制和神经传导)、肌肉收缩和神经兴奋与肌肉收缩的耦联都是以电活动为基础。电刺激是指用特

一个产品带有CE 标志(标记) 也就意味着其制造商宣告:该产品符合欧洲的健康、安全、与环境保护之相关法律中所规定 的基本要求。因而该产品是对:使用者(译者注:人)、宠物(

江苏省2021年医疗器械临床试验监督抽查项目 序号 备案号 试验用医疗器械名称 申办者 临床试验机构 1 苏械临备20190008 连续血糖监测系统 南通九诺医疗科技有限公司 南京大学医学院附
3月13日,西门子医疗Corindus途灵™最新一代CorPath®GRX介入手术机器人在海南博鳌超级医院完成其国内首例机器人辅助下冠状动脉介入治疗(PCI)手术,手术由中国科学院院士、复旦大学附

按照中共中央办公厅和国务院办公厅印发的《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》(厅字〔2017〕42号)和《国务院关于修改〈医疗器械监督管理条例〉的决定》(

体外诊断试剂临床试验数据造假行为,怎么处罚?本文针对体外诊断试剂注册环节的临床试验数据造假行为,一起来看看惩罚力度。

2020年11月9日,广东省药品监督管理局发布《关于调整广东省医疗器械注册审评补充资料预审服务的通告》,详见正文。"
六年
医疗器械服务经验
联系思途,免费获得专属《落地解决方案》及报价
咨询相关问题或咨询报价,可以直接与我们联系
思途CRO——医疗器械注册临床第三方平台