【国家化妆品备案查询】国家化妆品备案查询网站入口
2020年8月14日,化妆品备案网系统和检测系统更新了!国家化妆品备案查询需要移步到新网址了!
来源:医疗器械注册代办 发布日期:2021-03-14 阅读量:次
消字号是我国卫生消毒用品的专用批准文号,属于卫生行政部门管理的非药品类产品,主要包括消毒剂、消毒器械和卫生用品三大类。这类产品仅具备消毒、抑菌或杀菌功能,不能宣称任何治疗效果,其检测指标需符合《消毒技术规范》等国家标准。例如,常见的84消毒液、紫外线消毒灯、女性抗菌洗液等均属于消字号范畴。与药品(国药准字号)不同,消字号产品由省级以下卫生行政部门审批,申报周期短、费用低,但需严格遵循备案管理要求。

申请主体限制:个体工商户或个人不得申请消字号备案,必须是具备独立法人资格的企业或工厂,例如生物科技公司、制药企业等。
生产资质要求:若企业自主生产,需取得《消毒产品生产企业卫生许可证》;若委托生产,需与受托方签订合同并提供其生产资质证明。
人员与设施:企业需配备专业卫生管理人员,生产场地布局、工艺流程需符合《消毒产品生产企业卫生规范》,从业人员需通过健康检查与卫生知识培训。
禁用成分:配方中严禁添加抗生素、抗真菌药物、激素等处方药成分,以及卫生行政部门公布的禁用物质(如部分化学防腐剂)。原料需符合《中国药典》《化妆品安全技术规范》等标准,例如酒精浓度、植物提取物纯度等。
配方审核重点:消毒剂需明确有效成分含量及作用机理;抗(抑)菌洗剂需提交完整配方;消毒器械需提供结构图或元器件清单。若涉及食品相关用途(如餐具消毒剂),还需额外检测铅、砷等重金属残留。
消字号产品按风险等级分为三类,备案要求差异显著:
1. 消毒剂与消毒器械:
- 第一类(高风险):包括用于医疗器械灭菌、皮肤黏膜消毒的产品,需提交卫生安全评价报告(含理化指标、微生物杀灭试验、毒理试验等),并向省级卫生部门备案。
- 第二类(中风险):如环境消毒剂,备案时需检测有效成分含量、pH值、稳定性及杀菌效果。
2. 卫生用品:如湿巾、抗抑菌凝胶等,备案材料包括产品标签样稿、检验报告、生产许可证复印件等,检测项目涵盖微生物指标、刺激性试验等。
检测机构资质:检测须由CMA(中国计量认证)或CNAS(中国合格评定国家认可委员会)认可的第三方实验室完成。
核心材料清单:
- 产品配方或器械结构图
- 生产工艺流程图
- 检验报告(需加盖检测机构骑缝章)
- 标签及说明书样稿(禁止标注“治疗”“消炎”等违规宣称)
- 企业营业执照与生产许可证
- 卫生安全责任保证书
备案流程:
1. 材料准备:明确产品类别与检测项目,起草企业标准或质量标准。
2. 样品送检:同一批次样品需完成所有检测项目,如消毒剂需进行加速稳定性试验(37℃保存90天)。
3. 网上申报:通过省级卫生健康委员会备案系统提交材料,涉密资料可线下补充。
4. 形式审查:卫生部门在5个工作日内完成审核,通过后发放备案凭证。
备案延续要求:第一类产品卫生安全评价报告有效期为4年,到期前需重新检测并提交材料;第二类产品报告长期有效,但若配方、工艺变更需重新备案。
1. 宣传合规:产品包装及广告中不得出现“治疗”“药用”等误导性词汇,仅可标注“抑菌率≥90%”等实测数据。
2. 标签规范:需标注生产企业名称、生产日期、有效期、执行标准号及“消字号”批准文号(格式为省简称+卫消证字+年份+编号)。
3. 委托生产风险:委托方需对产品质量全程负责,若受托方生产条件不达标,备案可能被撤销。
通过系统化备案管理与严格自查,企业可有效规避违规风险,确保产品合法上市。

站点声明
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
思途医疗科技有限公司专注于医疗器械产品政策与法规规事务服务,提供产品注册备案申报代理、临床试验、体系建立辅导、分类界定、申请创新办理服务。

2020年8月14日,化妆品备案网系统和检测系统更新了!国家化妆品备案查询需要移步到新网址了!

目前化妆品都要求必须进行备案的,如果不备案就是违法的情况。所以必须进行备案。已经拿到资质的化妆品备案编号在哪里找?怎么找?本文分享常见的化妆品备案编号查询方法。

SSU是Study Start Up的缩写,从最初的项目准备,到启动访视(Site Initiation Visit)之前所有的准备工作,对整个临床研究项目的启动非常关键。负责这个关键阶段工作的部门人员,就叫做SS

消字号”产品指的是消毒产品,主要用于杀灭或清除传播媒介上的病原微生物,是卫生部为提高公共卫生质量而批准的一类产品。由省一级卫生主管部门审核批准,是经过卫生部门批准

初次申请消字号备案,总会遇到磕磕绊绊的问题,常见的有申请流程、申请资料、申请周期等问题,本文将对申请消字号产品流程及费用简单概述,对即将进入消毒产品行业的企业做一
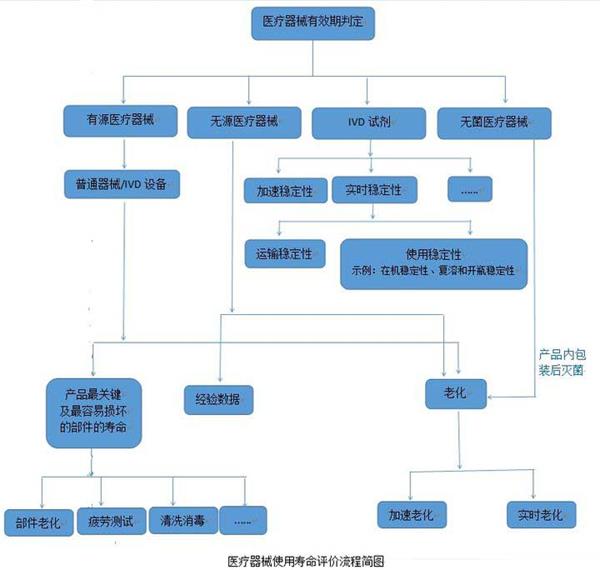
医疗器械的使用寿命是指医疗器械从规划、设计、生产、销售、安装调试到使用、维修、维护检测、报废的全过程。而医院使用的医疗器械的应用质量和安全管理在整个寿命过程中占重

你是否遇到过这样的问题,国产化妆品小品牌不少,怕买到假冒伪劣产品,现在的仿造化妆品也不少,外包装还同样有防伪标签,就很头疼。那么,查询国产非特殊用途化妆品备案信息

化妆品分为国产和进口、又分为非特殊化妆品和特殊化妆品,备案的费用和周期各不相同,具体各类化妆品备案多少钱?周期要多久?看完就懂了......

临床试验从筛选到立项、启动、入组和中心关闭是一个完整的闭环,什么时候可以开始关闭中心?关闭中心需要做哪些事情?从哪里着手?今天我们就来谈一谈临床试验关中心阶段的那

在临床试验方案的设计过程中,大家都会尽可能的考虑到各种可能影响试验的因素,并制定标准操作规程,尽量避免和减少在试验中可能出现违背及偏离方案的情况发生,但在试验的执
六年
医疗器械服务经验
联系思途,免费获得专属《落地解决方案》及报价
咨询相关问题或咨询报价,可以直接与我们联系
思途CRO——医疗器械注册临床第三方平台