MDD和MDR比较|欧盟医疗器械新法规MDR有哪些变化?
本文介绍了欧盟医疗器械新法规MDR相比于将替代的MDD法规的几点新增要求。建议收藏学习。明年5月份起,Medical Devices Regulation(MDR)(2017/745/ EU)将替代原本的Medical Devices Directive (93
来源:医疗器械注册代办 发布日期:2024-10-25 阅读量:次
2024版《赫尔辛基宣言》已于前几日正式发布,与老版本相比,有哪些变化呢?下面内容出自作者新猫,一起来看看吧。

2024 修订版将“受试者(subject)”调整为“参与者(participant)”。这一变化体现了对参与医学研究个体身份认知的转变,强调其在研究中的主动参与性和积极性,而不仅仅是被动接受试验的对象。这种表述的变化有助于提升参与者的主体地位,使他们在研究过程中更能积极地表达自己的意见和需求,也提醒研究者更加尊重参与者的意愿和权益。
更多关注特殊群体的“脆弱性(vulnerability)”。特殊群体包括儿童、孕妇、老年人、残疾人、精神疾病患者等,由于自身的生理、心理或社会地位等原因,在医学研究中可能更容易受到伤害或不公正对待。强调脆弱性意味着在研究的设计、实施及伦理审查等各个环节,都要更加谨慎地考虑特殊群体的特点和需求,采取额外的保护措施,确保他们的权益不受侵犯。
知识产出与个人权利的平衡:以往的版本强调医学研究的目的是为了产出知识,以了解疾病、改进干预措施并增进健康等,修订版明确地指出这些目的绝不能凌驾于研究参与者个人的权利和利益之上。进一步突出了对参与者权益的优先保护,即使医学研究具有重要的科学意义和潜在的公共利益,如果对参与者造成的风险过大或损害了他们的权利,也不应进行。这一变化使得研究目的与参与者权益之间的关系更加清晰,为研究者在决策时提供了更明确的指导原则。
增强与参与者及其社群的互动:修订版更加注重在医学研究开展前、中、后,与潜在和已入组的参与者及其社群进行有意义的互动。这包括让参与者及其社群能够分享他们的优先事项和价值观,参与研究的设计、实施和其他相关活动,并参与理解和传播研究结果。强调了参与者及其社群在研究过程中的参与度和影响力,有助于提高研究的科学性、合理性和社会可接受性,同时也能增强参与者对研究的信任和支持。
进一步明确了医生和其他研究者在开展涉及人类参与者的研究时,保护研究参与者的责任必须始终由他们承担,绝不能由研究参与者承担,即使参与者已经同意。这一规定强调了研究者的专业责任和道德义务,即使在参与者自愿参与的情况下,研究者也不能减轻或推卸对他们的保护责任。这有助于防止研究者因各种原因而忽视或放松对参与者的保护,确保参与者的生命、健康、尊严、自主性、隐私等得到充分的保护。
近年来突发公共卫生事件频发,修订版对在突发公共卫生事件期间进行医学研究的伦理原则进行了特别的规定和强调。例如,在紧急情况下如何平衡研究的紧迫性与伦理要求,如何确保参与者的权益在快速推进的研究中不受损害等。这使得《赫尔辛基宣言》更能适应复杂多变的现实情况,为在特殊时期进行医学研究提供了伦理指导。
《赫尔辛基宣言》的修订,反映了国际社会对医学研究伦理的高度重视和不断探索,对于保护人类参与者的权益、推动医学科学的健康发展具有重要意义。
以上仅为个人学习心得,望听取前辈同仁指导。

站点声明
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
思途医疗科技有限公司专注于医疗器械产品政策与法规规事务服务,提供产品注册备案申报代理、临床试验、体系建立辅导、分类界定、申请创新办理服务。

本文介绍了欧盟医疗器械新法规MDR相比于将替代的MDD法规的几点新增要求。建议收藏学习。明年5月份起,Medical Devices Regulation(MDR)(2017/745/ EU)将替代原本的Medical Devices Directive (93

随着医疗器械分类及免临床医疗器械目录的调整,部分电子内窥镜产品的管理类别从III调整为II类,同时列入免于进行临床试验的医疗器械目录,因此在注册申报过程中,其注册申报要求
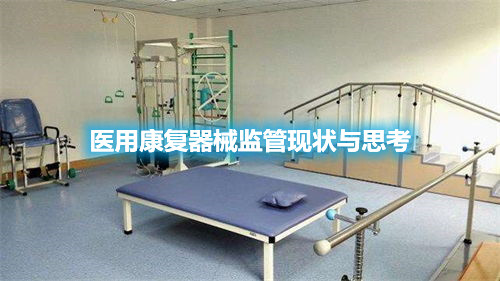
据统计,我国是世界上医用康复器械需求人数最多、市场潜力最大的国家。近年来我国康复医疗器械产业迎来爆发式增长,医用康复器械产品种类繁多,使用对象数量庞大,新技术新产

2020年12月21日,国务院常务会议审议通过了《医疗器械监督管理条例(修订草案)》(以下简称《修订草案》),意味着医疗器械行业母法第三次大修改即将接近尾声。这次修改是在医疗

2024年全国医疗器械展会一览序号展示名称时间地点网址12024歌华医药健康产业(济南)博览会3.13-3.14山东·济南https://www.ghyjh.com/22024第7届中国(浙江)国际医疗器械展览会3.14-3.16浙江·杭州http://www.cimde.com.cn/32024长三角国际康复设备与训练器材展览会3.14-3.16浙江·杭州www.rete-exbo.com420

为加强医疗器械产品注册工作的监督和指导,进一步提高注册审查质量,国家药品监督管理局组织制定了《医疗器械动物试验研究注册审查指导原则 第一部分:决策原则(2021年修订版)

昨天写了一篇自己关于赫尔辛基宣言的理解,被网友提醒:尊重从改变称谓开始,新版“参与者”vs旧版“受试者”。所以抓紧学习了新版宣言,并重点研习了这一块,今天就来分

2024年10月19日,在第 75 届世界医学会全体大会上正式通过了《赫尔辛基宣言》的最新修订版本;《赫尔辛基宣言》作为人类参与者的医学研究伦理原则,必将为全球

在医疗器械行业,持续关注行业信息对于从业者来说至关重要。无论是了解市场趋势、跟踪政策法规,还是学习技术和创新,关注行业信息都能为从业者带来诸多好处。本文将探讨关注行业信息的重要性,并分享一些值得关注的公众号,帮助医疗器械从业者更好地获取行业资讯,提升自身的专业水平。为什么要关注行业信息1-了解市场趋势和竞争情况: 关注行业信息可以帮助医疗器械从业者了解市场的发展趋势、消费者需求和竞争格局,有助于制

关于公布2024年下半年人类遗传资源行政许可审批受理截止时间计划的通知为进一步提高人类遗传资源行政许可审批的服务质量,方便申请者了解审批进度,现将2024年下半年人类遗传资源行政许可审批受理截止时间计划公布。以下受理截止时间均为当天16:30,如遇特殊情况需调整时间,将提前进行通知。批次受理截止时间2024年第13批2024年06月27日2024年第14批2024年07月11日2024年第15批2
六年
医疗器械服务经验
联系思途,免费获得专属《落地解决方案》及报价
咨询相关问题或咨询报价,可以直接与我们联系
思途CRO——医疗器械注册临床第三方平台