医疗器械文件(MDF)和医疗器械主记录(DMR)是什么?
随着医疗器械出口的日益增长,根据市场的需求各医疗器械生产厂商需要符合国家和地区的质量体系法规越来越多,所以经常会碰到出处于不同法规或标准的一些比较容易混淆的概念及
来源:医疗器械注册代办 发布日期:2025-07-18 阅读量:次
先看看国家是怎么规定的。电子病历这事儿,国家有明确要求。核心的文件是《电子病历基本规范》。它说电子病历是医务人员用医院信息系统生成的文字、图表、影像这些数字化信息,能存、能管、能传、能看。注意啊,用Word打出来再打印的病历,不算电子病历。

医院建了电子病历系统,那住院病历、门诊病历这些主要的医疗记录,就得用这个系统来做。这是《电子病历基本规范》的基本要求。 招标文件也写得明明白白,电子病历系统得满足《病历书写基本规范》、《电子病历基本规范》这些要求。做电子病历的厂商,还得有相关的软件著作权证书。 以前有人担心电子病历改了不认账,打官司没用。但现在技术和管理跟上了,国家也认可了电子病历的法律地位,关键是要用合规的系统。
重点来了,你提供的这个情况特别关键:以患者为受试者的临床试验,相关医疗记录要记到门诊或住院病历里。如果医院有电子病历系统,研究人员就得用这个系统来记录受试者的医疗信息。要是没用,得有个站得住脚的理由。 这个要求很实在。
为啥这样规定呢?首先,受试者首先是病人,他在医院看病产生的所有记录,就该按医院的规定来。医院既然建了电子病历系统,记录就该走这个系统,这样统一管理,不容易出错,也方便以后查。用电子病历系统,能解决手写病历乱、管不好的老问题,对保证医疗质量有好处。 其次,临床试验数据要真实可靠。把受试者的医疗信息直接记在医院的电子病历系统里,而不是单独搞一套,更能保证记录的完整性和可追溯性,减少记录不一致的风险。简单说,就是更靠谱。
那“适当理由”是啥?这个得具体问题具体分析。比如,医院的电子病历系统突然坏了,正在修,那暂时不用情有可原。或者,某个检查项目特别特殊,电子病历系统暂时不支持记录这种格式的数据,那也得想办法先记下来。但不管啥理由,都得有记录,说明为啥不用电子系统,后面该补的还得补上,不能糊弄。系统维护这事儿,医院招标时也会考虑进去。
说到底,不是医院里每一张纸片都得塞进电子病历系统。但只要是和病人看病直接相关的、属于门诊或住院病历范畴的记录,特别是涉及病人诊断、治疗这些核心医疗过程的记录,医院有电子病历系统的话,就必须用它来做。
临床试验这块更要重视。 受试者的医疗信息,是病历的一部分,医院有电子病历系统,研究人员没理由不用。除非真有特殊情况,比如系统临时故障或者功能确实不支持,但这得是例外,要有记录有解释。思途CRO在协助客户做临床试验时,也会特别关注这点,确保记录方式合规。
国家政策是鼓励推广电子病历的,这方向不会变。 用电子系统记录,对医院管理、医疗质量、还有像临床试验这种需要严谨数据的事儿,好处是实实在在的。所以,回到问题本身:医院建了电子病历系统,那核心的医疗记录,包括临床试验中受试者的相关医疗信息,原则上都该通过这个系统记录。不用,那得是真有说得过去的特殊情况才行。

站点声明
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
思途医疗科技有限公司专注于医疗器械产品政策与法规规事务服务,提供产品注册备案申报代理、临床试验、体系建立辅导、分类界定、申请创新办理服务。

随着医疗器械出口的日益增长,根据市场的需求各医疗器械生产厂商需要符合国家和地区的质量体系法规越来越多,所以经常会碰到出处于不同法规或标准的一些比较容易混淆的概念及

电子数据采集(electronic data capture,EDC)是电子化临床试验的重要组成部分。EDC通过计算机、局域网、因特网、PDA和各种便携式设备、互动式语音或网络应答系统及远程数据输人(remoted
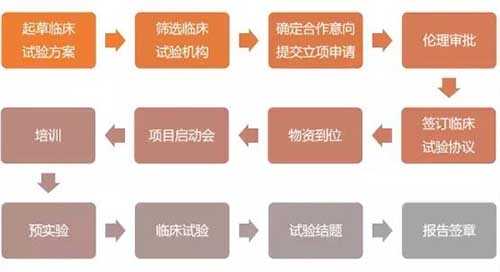
新冠肺炎疫情发生以来,相关药械企业为满足诊断需求,加速研发生产新冠肺炎诊断产品;特别是作为确诊新冠肺炎的主要产品——体外诊断试剂,国家药监部门对其注册申请启动了应

本文章主要从笔者作为CRA在SSU阶段进行合同拟定以及推动审核过程中积累的心得,来跟大家分享下,如有错误地方,请大家多多指教~
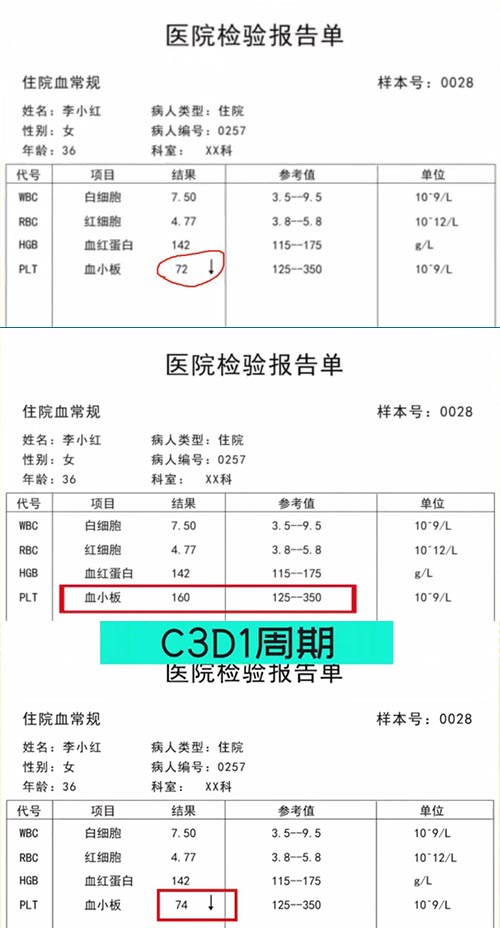
某乳腺癌项目012号受试者,基线期血小板计数降低II级,研究者判断有临床意义,并将血小板计数降低记录在病史之中。C2D15周期用药前实验室检查显示恢复了正常水平,然后在C3D1周期用

今天主要是忍不住给大家安利一个好用的东西—真实世界数据(Real World Data,RWD)。NMPA在2020年11月年发布了《真实世界数据用于医疗器械临床评价技术指导原则(试行)》。其实,这个

家庭中常用的餐巾纸、湿巾、婴幼儿纸尿裤、成人纸尿裤、纸尿布、隔尿垫、卫生巾、卫生护垫、化妆棉、消毒剂、空气消毒器械等都属于消毒产品。哪些产品需要办理消字号备案?哪

当申办方和CRO向研究中心提供一长串产品和平台时,他们往往会忽视个别研究中心的独特需求和偏好,而倾向于一刀切的选择。研究中心的研究团队已经承受了巨大的时间和劳动负担。

你知道申办方和研究者的医疗器械临床试验记录各有什么要求吗?如实填写记录是基本要求,其他要求又有哪些呢?我们一起来看一下医疗器械临床试验记录与报告方面的要求。

实验室原始记录用于为可追溯性提供文件、并提供验证、预防措施和纠正措施的证据,具有清晰、完整、真实和原始等特点。它们是出具检定证书,校准报告的依据。重要性不多说,总
六年
医疗器械服务经验
联系思途,免费获得专属《落地解决方案》及报价
咨询相关问题或咨询报价,可以直接与我们联系
思途CRO——医疗器械注册临床第三方平台