有源医疗器械加速老化试验效期验证及使用期限验证流程
为了确保医疗器械在生命周期内的安全及有效性,注册人应在设计开发中对其使用期限予以验证。使用期限的验证是医疗器械可靠性研究的重要组成部分,制定并验证合理的使用期限有
来源:医疗器械注册代办 发布日期:2023-07-06 阅读量:次
第二类医疗器械是指使用医疗技术,对人体进行预防、诊断、治疗、矫形或者缓解疾病、损伤或残疾的器械,其安全性和有效性需要严格控制和监管。第二类医疗器械是最具代表性的医疗器械,涉及的范围广泛,可以分为以下几类:

1、诊断类器械
诊断类器械用于疾病诊断、判定疾病病情、监测生理指标等,是医学检查、诊断中必不可少的设备。常见的诊断类器械包括血糖仪、血压计、血氧仪、体温计、胆固醇测试仪、心电图机、脑电图机、超声诊断仪、放射线诊断设备等。
2、治疗类器械
治疗类器械用于医疗、治疗、护理等,是医疗过程中重要的辅助设备。常见的治疗类器械包括心脏起搏器、呼吸机、输液泵、体外循环设备、雾化器、拔罐器等。
3、手术类器械
手术类器械是外科医生在手术中使用的医疗器械,主要包括手术刀、手术钳、缝合针、骨科手术器械、胸腹腔镜等。手术类器械具有高度的技术含量和安全风险,需要医生具备专业的技能和经验才能操作。
4、植入类器械
植入类器械是医生在手术过程中植入人体的医疗器械,主要用于人体的矫形、修复、替代等。常见的植入类器械包括人工髋、人工膝、心脏支架、人工耳蜗、心脏瓣膜、人工晶状体等。植入类器械具有高度的技术含量和风险,需要医生具备专业的技能和经验才能操作。
5、体外诊断试剂
体外诊断试剂是用于检测人体内生物标志物或特定物质的试剂,包括了广泛的检测项目,例如检测血糖、肝功能、肾功能、癌症标志物、心脏酶、免疫学、细菌和病毒等。这类器械广泛应用于医疗领域、药物研发、生命科学等领域。
6、支持类器械
支持类器械包括医用氧气、医用压缩空气、吸痰器、氧气袋、呼吸面罩、呼吸管等。这些器械主要用于支持呼吸、血液循环等生命体征,可以帮助病人维持生命体征的稳定,是医疗急救中必不可少的设备。
7、牙科器械
牙科器械是用于口腔疾病治疗、口腔修复、牙齿矫正等的设备。常见的牙科器械包括牙科手术钳、牙钻、口腔护理器具、牙齿美白器等。
8、其他器械
此外,还有一些不属于以上类别的第二类医疗器械,例如透析机、体外循环设备、计算机辅助手术设备、医疗照明设备等。
总体来说,第二类医疗器械涵盖了医疗领域中最重要的设备,涉及的范围广泛,是保障人类健康和生命的必备品。同时,由于这类器械具有较高的技术含量和安全风险,对其安全性和有效性的严格监管也显得尤为重要。

站点声明
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
思途医疗科技有限公司专注于医疗器械产品政策与法规规事务服务,提供产品注册备案申报代理、临床试验、体系建立辅导、分类界定、申请创新办理服务。
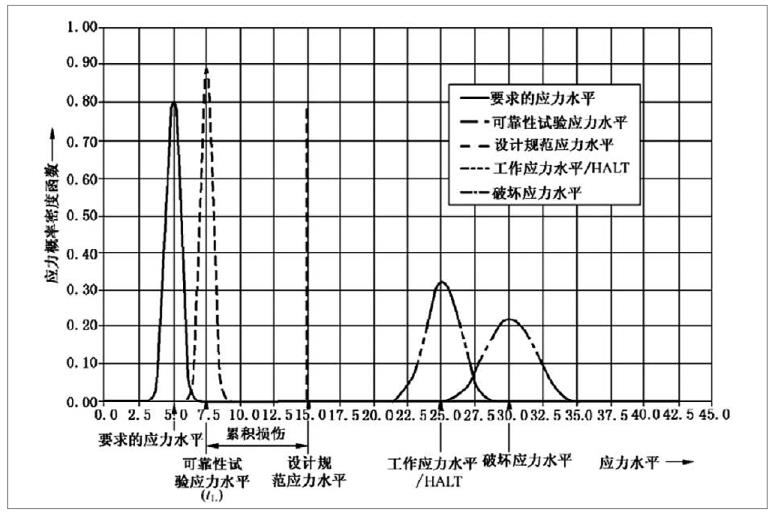
为了确保医疗器械在生命周期内的安全及有效性,注册人应在设计开发中对其使用期限予以验证。使用期限的验证是医疗器械可靠性研究的重要组成部分,制定并验证合理的使用期限有

随着国家医疗改革的不断深入,使得综合性大中型医疗机构的中心实验室对自动化系统有了新的要求,为了简化检测流程,提高检测效率,保证数据准确度等,中心实验室对集中化诊断

润滑剂类产品在美国根据产品预期用途的不同主要分为人体润滑剂和患者润滑剂:其中,人体润滑剂主要成分为水、丙二醇、羟乙基纤维素、苯甲酸、卡波姆、氢氧化钠等,作用于生殖

中国能排进世界十大医疗器械制造强国吗?暂时还不能,因为排进前十的国家都有许多知名械企和世界级医疗器械巨头;而中国比较出名的可能只有迈瑞了,其他械企仍需努力了。下面

本文介绍了欧盟医疗器械新法规MDR相比于将替代的MDD法规的几点新增要求。建议收藏学习。明年5月份起,Medical Devices Regulation(MDR)(2017/745/ EU)将替代原本的Medical Devices Directive (93

FDA于2020.12.11发布了关于简短(Abbreviated) 510(k)申请的相关产品指南,该指南是在遵守“基于安全有效性途径”这一前提下编制提出的。在这个框架下,申请人若计划使用安全有效性途径提交
可吸收高分子材料介绍,及其在植入医疗器械中的应用。1、植入产品的定义国家食品药品监督管理局《医疗器械分类规则》(局令第15号)第八条中对“植入器械”的定义为:任何借助

生物材料在疾病治疗和医疗保健中发挥了重要的作用,按材料性质,生物材料可分为惰性材料与可降解性材料两种,目前生物材料的发展呈现出由惰性向可降解性(水解和酶降解)转变的趋

医疗器械注册费是行政性收费,按照注册单元收取,部分省份不收取医疗器械注册费用,绝大部分省份还是收取的。本篇文章统计了截止到2022年1月5日各地医疗器械注册收费标准。

一个产品带有CE 标志(标记) 也就意味着其制造商宣告:该产品符合欧洲的健康、安全、与环境保护之相关法律中所规定 的基本要求。因而该产品是对:使用者(译者注:人)、宠物(
六年
医疗器械服务经验
联系思途,免费获得专属《落地解决方案》及报价
咨询相关问题或咨询报价,可以直接与我们联系
思途CRO——医疗器械注册临床第三方平台