药物临床试验的成本在多少?Ⅲ期临床要花多少钱?
发布日期:2023-10-10 阅读量:次
前言:将新药推向市场和进行临床试验的成本是制药公司关注的核心问题,由于临床开发计划更加复杂,制药公司应对临床试验成本逐年上升。造成这种复杂性的因素包括监管审查的加强,越来越需要证明新药的安全性和有效性,以及在确定的患者亚群或患有罕见疾病的患者中进行试验所面临的挑战。
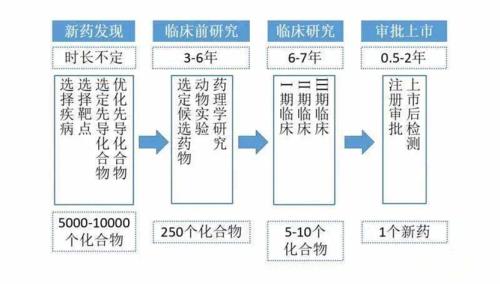
为了向公司提供临床试验成本的参考标准,KMR集团在2016年进行了具有里程碑意义的临床试验成本研究,评估了7家主要制药公司在2010年至2015年期间进行的700多项临床试验的临床试验成本。这项评估为主要生物制药公司的高级管理层提供了可靠的跨行业成本数据,以便他们能够评估其运营效率,做出更准确的财务预测,以及更有效地评估许可和资产收购的成本负担。
成本分析
总的试验费用按每项试验的关键成本领域细分:人员、外购、对外援助项目合同和其他费用。图1显示了这些区域中每个区域在III期临床试验的数据集中的比例。人员支出占第三阶段平均试验总费用的37%,而外购和对外援助项目合同费用分别约占总试验费用的20%左右。
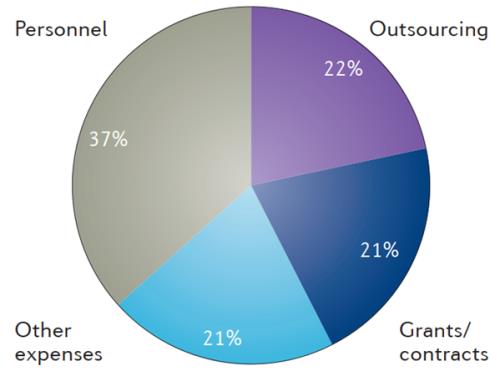
图1 III期临床试验费用的组成部分
这些数据使成本绩效可通过三种方式进行评估:第一,将一家公司的临床试验成本组合与整个集团的临床试验成本组合进行比较,以更好地了解其成本概况与同行的不同之处;第二,评估给定公司的试验组合相对于其特定治疗领域重点的成本;第三,从运营效率的角度检查试验成本概况。
临床试验的中位值
对于数据集中的试验,从方案批准到最终临床试验报告进行一项研究的成本中值为:I期临床试验的中位值成本为340万美元,II期临床试验的中位值成本为860万美元,III期临床试验的中位值成本为2140万美元(图2)
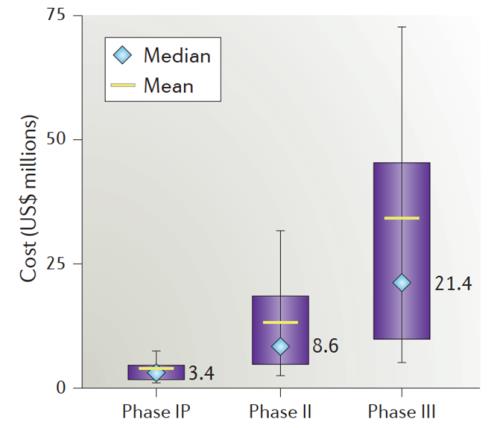
图2 临床试验成本
这些费用与试验方案设计的选择和受试者的数量、地点和访问等因素有关(P≤0.0001)(表1)。研究者还使用统计技术来确定影响成本的关键因素,这些因素基于公司的战略选择,例如对进行临床试验国家的选择。增加国家数量和使用新兴市场会增加成本(表1)。与较高成本相关的另一个关键因素是试验持续时间(表1)。特别是,第三阶段试验每增加一个月,花费的中位数为671,000美元。以此为基准,即使是很小的周期时间减少也可能对整个临床开发预算产生重大好处。
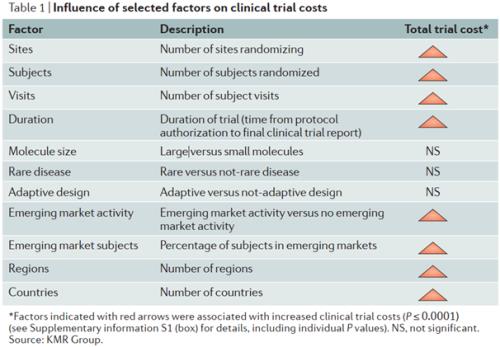
还有一些因素对总体试验成本没有统计学上的显著影响,例如试验是否使用适应性设计,是针对一种罕见疾病还是涉及一种生物制品(表1)。然而,尽管罕见疾病研究与总试验成本的差异无关,但它们确实在统计学上显著(P=0.0003)地增加了每个受试者的拨款成本,部分原因是患者池较小,设计更复杂。同样,大分子研究的每个受试者的拨款成本也显著较高(P=0.004)。
运营业绩
尽管设计因素对任何成本评估都是必不可少的,但它们并不能说明公司的运营业绩。为了评估运营绩效,研究者使用多元回归得出了一个统计模型,使用以下核心临床试验设计参数:研究规模、治疗区域和治疗持续时间。
一般而言,有三大类因素可以针对改善成本效益:试验设计参数的选择(如研究规模、终点数量和治疗持续时间)、操作选择(如外购和使用新兴市场)和缩短周期时间。了解所有因素之间的关系对于做出最佳选择是至关重要的。
III期临床试验的费用
据估计,如果将研发失败、批准后研究和机会成本考虑在内,药物开发的成本是4300万美元到29亿美元不等。研究人员采取了不同的方式来理解这些数字,更加关注关键试验的成本。他们在《JAMA Internal Medicine》杂志上报道,在评估了2015年至2016年FDA批准的59种新药的138项关键试验的细节后,得出一项III期临床试验的费用中位值为1900万美元。总体来说,估算与KMR集团的分析是一致的。
研究人员发现,临床试验成本差异往往很大(根据IQVIA合同研究组织的成本计算器估计)。一项有四名患者参加的III期临床试验,测试Wellstat的尿苷三醋酸酯治疗罕见的遗传性代谢紊乱或酸尿症,可能只需要大约200万美元。但诺华公司有8,442名患者参加的Sacubitril/valsartan与enalapril的非劣效性试验(Non-inferiority Trial, NIT),观察了住院和心血管死亡率结果,可能耗资约3.47亿美元。
作者总结道:“不同于广泛存在的假设,我们的研究提供了一种不同的视角,即复杂和昂贵的临床试验是开发新药成本高的主要原因。这些数据表明,会进行高成本试验,但通常是在药物作用较小或已知药物已经提供临床益处的情况下进行的。另一方面,对具有显著临床益处的新药进行关键试验能够以较低的成本进行。
参考文献:
[1] Martin, L.,Hutchens, M., Hawkins, C. et al. How much do clinical trials cost?. Nat RevDrug Discov 16, 381–382 (2017). https://doi.org/10.1038/nrd.2017.70
[2] Mullard, A.How much do phase III trials cost?. Nat Rev Drug Discov 17, 777 (2018). https://doi.org/10.1038/nrd.2018.198

站点声明
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
郑州思途医疗科技有限公司专注于医疗器械产品政策与法规规事务服务,提供产品注册备案申报代理、临床试验、体系建立辅导、分类界定、申请创新办理服务。
行业资讯
知识分享





 豫公网安备 41010202003160号
豫公网安备 41010202003160号